新冠疫苗的快速开发重塑疫苗科学

Pfizer与BioNTech合作的在美国的第一批 COVID-19疫苗已经准备发货。
用于解决SARS-CoV-2的快速方法可能会改变疫苗科学的未来。
2020年初,当科学家开始为SARS-CoV-2冠状病毒寻找疫苗时,还比较保守,不敢断言能迅速取得成功。从病毒取样到批准,以前病毒疫苗最快的获批时间是4年,例如1960年代的腮腺炎疫苗。去年科学家们还认为,2021年夏天新冠疫苗能获批已经是很乐观的估计了。
但是到2020年12月初,几种疫苗的开发者纷纷宣布了大型临床试验中获得的喜人结果,并表示它们显示了更大的潜力。12月2日,药品巨头Pfizer公司与德国生物技术公司BioNTech合作生产的疫苗,成为首个经过全面测试的、获准用于紧急用途的疫苗。
盖恩斯维尔佛罗里达大学(University of Florida)的生物统计学家Natalie Dean表示,这种开发的速度“挑战了我们开发疫苗的可能性的整个范式”。是否可以在同样短的时间内开发出其它疾病的疫苗?这一想法充满吸引力。很多疾病的疫苗也是人们迫切需要的,例如疟疾、结核病和肺炎等疾病每年一共杀死数百万人,研究人员还预计未来会有更多致命的传染病。
马萨诸塞州波士顿哈佛医学院(Harvard Medical School)病毒学和疫苗研究中心(Center for Virology and Vaccine Research)主任Dan Barouch指出,COVID-19的经验几乎肯定会改变疫苗科学的未来。这表明,在真正的全球紧急情况和足够的资源下,疫苗开发可以快速进行。新的疫苗生产的方法,例如使用信使RNA(mRNA),已经在COVID-19疫情中得到了验证。这表明,在不损害安全性的前提下,疫苗开发过程可以大幅加速。
得益于以前对相关病毒的研究以及制造疫苗的更快方法,全世界才能够如此迅速地开发出COVID-19疫苗。巨大的资金投入,使公司可以并行进行多个试验,并且监管机构的行动比正常情况下更迅速。其中一些因素也可用于其它疫苗的开发工作,尤其是更快的生产平台。
但是并不能保证其它疫苗的开发也能如此迅速。只有在拥有同样的巨额资金投入,类似的社会和政治紧迫感时,才能重现这种快速的疫苗开发情况。同时,开发速度也将取决于病原体的性质。科学家要庆幸的是,SARS-CoV-2是一种变异相对较慢的病毒,且恰好属于一个经过充分研究的病毒家族。
多年的研究进展
推动新冠疫苗开发的研究很早就开始了。多年来,研究人员一直在关注引起非典肺炎的相关冠状病毒,这些冠状病毒能引起SARS(严重急性呼吸道综合症)和MERS(中东呼吸综合症),并且在研发针对它们的疫苗——这些努力是如今新冠疫苗大获成功的基础。
常规疫苗包含病毒蛋白或病毒本身的失活形式,它们可刺激人体的免疫系统,抵抗这些病原物。但是在大规模(3期)临床试验中最先宣布有疗效的前两种COVID-19疫苗是基于脂质体包裹的mRNA。该mRNA编码SARS-CoV-2的关键蛋白——刺突蛋白。一旦这些mRNA进入人体细胞,人体就会产生这种蛋白质,也就是抗原——触发免疫反应的外来分子。Pfizer公司和BioNTech公司以及美国制药公司Moderna生产的疫苗都使用编码刺突蛋白的mRNA,该蛋白与宿主细胞膜上的受体结合,使病毒膜和细胞膜融合,使得病毒基因组得以进入人体并感染细胞。
康涅狄格州纽黑文市耶鲁医学院(Yale School of Medicine)致力于核酸疫苗(基于DNA或RNA长度的核酸疫苗)的研究已有20多年的免疫学家Akaki Iwasaki提醒,大量的前期投入才打造了现在的mRNA平台。DNA疫苗的基础研究至少在25年前就已经开始,而RNA疫苗得益于近10到15年的密集研究,其中一些研究聚焦于癌症疫苗。只能说,2020年刚好是天时地利人和。哪怕是5年前,RNA技术都尚未成熟。
例如,位于马里兰州贝塞斯达的美国国家过敏和传染病研究所(US National Institute of Allergy and Infectious Diseases, NIAID)的研究人员从对MERS和SARS的研究中知道,最好对RNA序列进行调节,以得到结构更稳定的刺突蛋白。NIAID疫苗研究中心副主任Barney Graham指出,如果可以将刺突蛋白表达成其原始的、融合前状态,它将变成一种更好的疫苗抗原。Moderna的合作者NIAID团队基于这方面的工作,在新冠疫苗的研发竞赛中,从1月份获得病毒基因组信息后就占据了领先地位。Dean表示,人们一直密切关注冠状病毒,这一事实确实使整个疫苗开发进程获得大大的加速。
由阿斯利康(AstraZeneca)制药公司与英国牛津大学(University of Oxford)联合生产的第三种疫苗在11月的3期临床试验中显示了功效,该疫苗不使用mRNA。相反,该疫苗使用携带编码SARS-CoV-2突刺蛋白的基因的病毒载体(或载体)。载体的选择也得益于多年的研究。该公司选择了一种从黑猩猩粪便中分离出的改良形式的腺病毒作为疫苗载体。伦敦卫生与热带医学学院疫苗中心(London School of Hygiene & Tropical Medicine)主任Beate Kampmann表示,此类常规疫苗的进步也来自对SARS、MERS、埃博拉和疟疾的研究,这种方法仍然比使用mRNA便宜。
Iwasaki指出,疫苗研究人员在很多方面都庆幸,这次疫情的元凶是SARS-CoV-2。这种病毒与艾滋病毒、疱疹甚至流感都不同,既不会发生巨大的突变,也没有有效的策略来削弱人类的免疫系统。比如,疱疹病毒具有更大的抵御能力——它可以主动阻止抗体结合,这使得寻找针对它的有效药物变得更加困难。流感病毒的快速突变需要在每个流感季节使用不同的疫苗制剂。
研发资金充裕
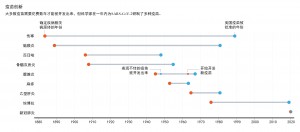
疫苗开发中最慢的步骤不是找到候选疗法,而是对其进行测试。这通常需要花费数年(图“疫苗创新”),公司会先对动物,然后对人类进行功效和安全性测试。人体试验需要三个阶段,这涉及不断增加的参与者数量和成比例增加的成本。COVID-19疫苗也进行了相同的试验,但投入的数十亿美元使公司愿意冒着财务上的风险同时进行一些试验(图“一年内开发出的疫苗”)。
GlaxoSmithKline公司疫苗部门的首席科学家Rino Rappuoli指出,有了公共资助者和私人慈善家向疫苗公司提供的巨额资金,研究人员就可以同时进行临床前和1、2和3期试验,以及并行进行制造,而不是按顺序进行。这意味着公司可以赌一把,对可能无效的候选分子也进行大规模测试和制造。Kampmann认为这完全降低了整个开发过程的风险。
她继续表示,没有这笔资金,疫苗科学不会产生如此快速的结果。埃博拉疫苗没有这么快问世,尽管该病毒在2014-16年间为非洲带来了毁灭性的灾难。埃博拉疫苗的研发花费了更长时间。只有在这次新冠疫情中,钱才到位。这是因为,不同于埃博拉,新冠疫情给所有国家,包括发达国家,都带来了经济灾难:这表明未来疫苗的开发,包括针对现有疾病(如疟疾)的疫苗开发还是不会这么快。Rappuoli指出,除非投入大量金钱,否则无法加速疫苗的开发。
得克萨斯州休斯敦贝勒医学院(Baylor College of Medicine)的病毒学家Peter Hotez表示,大型制药公司可能不仅受到了制止这种大流行的渴望的推动,还受到了政府资助其研发的机会的激励。Hotez提醒,美国空间机战行动(US Operation Warp Speed)疫苗计划的公共投资约为100亿美元,代表了制药公司有史以来最大的政府刺激方案。
事实上,推动力并非全部来自COVID-19大流行本身的紧迫性。以前的传染性和致死性病毒促使建立了国家和全球基础设施,以促进更快的疫苗开发。Graham指出,埃博拉病毒和寨卡病毒的爆发标志着全球如何更好地应对传染病危机的协调开始。如果2002年的SARS如此蔓延,我们当时没有这么先进的疫苗技术,也没有这样的协调系统,情况会比现在的疫情糟得多。
尤其是,2017年启动了流行病防范创新联盟(Coalition for Epidemic Preparedness Innovations, CEPI);它的目标是为快速、负担得起的疫苗开发提供必要的技术基础,这些疫苗针对几种已知具有流行潜力的病毒,包括MERS、埃博拉病毒和寨卡病毒。CEPI已部分资助SARS-CoV-2疫苗的工作,包括Moderna和牛津的疫苗。
在试验的最后阶段,COVID-19的普遍存在推动了疫苗的获批——因为公司需要有感染才能证明疫苗有效。当疾病本身不普遍时,很难进行功效试验——Dean指出,特别是在MERS等疫情中,疾病暴发是零散的,在某些地区达到高峰,而在其他地区则是低感染率。
COVID-19的经验可能还会促使监管机构重新考虑一些问题。尽管没有放宽对疫苗批准的严格标准,但首批候选疫苗大多是根据紧急使用法规批准的。这种批准方式更快,但是需要公司进行后续调查,以寻找副作用和持续的功效。国家监管机构还在2012年成立的、名为国际药物管理当局联盟(International Coalition of Medicines Regulatory Authorities)的全球机构的主持下,交换了有关COVID-19疫苗试验的信息。其目的是就疫苗试验的最佳终点等问题达成共识,以及在疫苗推出时如何协调对副作用的监控。
COVID-19疫苗研发对其它疫苗的益处
COVID-19大流行诱发了疫苗开发中一些永久性的变化。首先,mRNA疫苗——以前尚未批准将其用于人类——或许也能用作其它疾病疫苗。Kampmann认为这项技术正在革新疫苗学。候选mRNA疫苗可在几天内化学合成,而其它复杂的生物技术涉及在细胞中生产蛋白质。这项技术使敏捷的、即插即用方法可用于应对未来的流行病。
而且,Rappuoli指出,RNA大大简化了制造过程。你可以使用同一设施生产用于不同疾病的RNA。这减少了所需的投资。公司还应该提高生产能力,因为他们得一边生产COVID-19疫苗,一边得同时制造麻疹、小儿麻痹症和其它疾病的疫苗。这可能有助于满足将来的需求。
Hotez指出,COVID-19疫苗的大型临床试验以及其他正在开发中的试验,应提供对理解免疫反应更广泛有用的数据。鉴于所有不同的技术,以及收集的有关临床志愿者人口统计学、抗体和细胞反应的详细信息,今年我们能从人类疫苗反应中学到的知识可能比过去几十年加起来的都要多。人类疫苗学可以实现巨大的飞跃。
其它疫苗的快速开发,可能只有在发生大规模感染,相对迅速地进行大规模试验,并且投入大量资金时,才能实现。并且相比于SARS-CoV-2,其它病毒可能更难靶向。
研究人员表示,这就是为什么我们需要更多地了解所有病毒家族。Graham提醒,至少还有其它24个可以感染人类的病毒家族。与其等着浪费资源来抵抗下一个爆发的病毒,不如现在花钱来建立系统监视所有这些病毒,并生成有关每个家族的原型感染数据。
换句话说,没有坚实的基础科学平台作为基础,任何金钱投入都无济于事。Iwasaki表示,COVID-19疫苗的非凡成功很好地证明了科学可以迅速发挥作用,但这并不是一夜之间发生的。
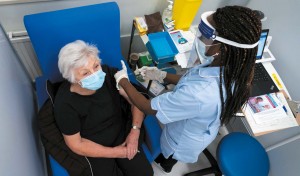
英国民众于12月初首次开始接种经过全面测试的COVID-19疫苗。
原文检索:
Philip Ball. (2021) The lightning-fast quest for COVID vaccines — and what it means for other diseases. Nature, 589: 16-18.
张洁/编译