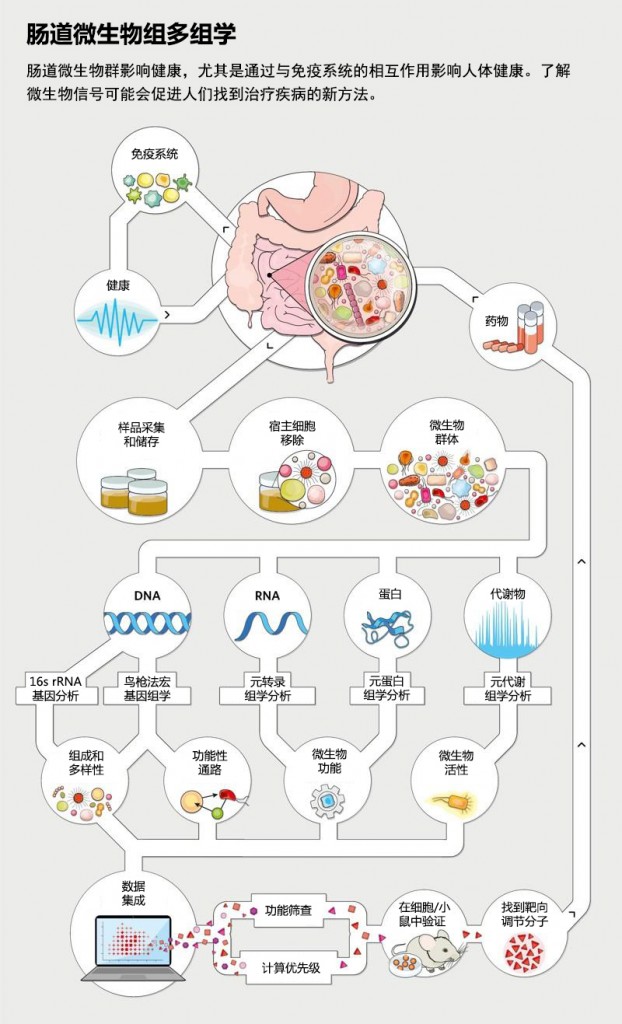
微生物组学如何促进人类健康
人类肠道中的微生物群是我们“第二基因组”(‘second genome’)的来源,而测序正在揭示它的秘密。
测序技术使对肠道微生物组的深入分析成为可能。研究人员现在可以探索人体内的微生物群落在做什么,以及它们如何促进或预防疾病。
微生物组研究正在改变我们看待自己作为人类的方式。人体拥有的微生物细胞至少和人体细胞一样多,我们的微生物基因目录中有超过100万个基因。然而,我们对大部分“第二基因组”的功能以及它如何影响健康仍然知之甚少。
Gary Schroth是位于圣地亚哥的Illumina测序技术开发公司的杰出科学家和副总裁,他指出,肠道微生物就像人体中的一个百搭器官,每个人都有不同的肠道微生物群,这对我们消化食物和代谢药物有巨大的影响。
大型合作项目,如美国的人类微生物组项目(Human Microbiome Project)和欧洲的MetaHIT(Metagenomics of the Human Intestinal Tract,人体肠道元基因组学),已经产生了大量有关特定疾病患者和健康人群肠道微生物群落的数据。这些项目揭示了个体间微生物的多样性,并强调了对微生物组进行更深入分析以了解其贡献的必要性。
肠道微生物群的紊乱与许多疾病有关,且不局限于那些影响消化系统的疾病,比如炎症性肠病(inflammatory bowel disease, IBD)。遗传性免疫介导疾病(如哮喘)、神经系统疾病(包括自闭症)以及遗传性疾病(如癌症)都与肠道菌群的失调有关。将微生物组研究转化为调节微生物组的治疗可以改变常见疾病的管理。
加州斯坦福大学(Stanford University)的物理学家Ami S. Bhatt认为,这是一个非常有吸引力的机会。几十年来,我们已经知道特定的人类基因突变与疾病有关,但解决这些问题真的很困难。然而,也有一些微生物组成与疾病有关,我们已经有有趣的工具来改变它们。
Bhatt的研究关注的不仅仅是微生物和人类细胞之间的交流,还有微生物群落内部的交流。据她解释,她们试图了解人体有哪些微生物,它们编码哪些产物,哪些产物可以作为通讯信号,以及随着时间的推移这些微生物如何变化。她的团队正在研究如何操纵这些信号来改善健康和病人的预后。
挖掘微生物群的技术
几十年来,基于序列的细菌分析依赖于编码16S核糖体RNA (rRNA)的基因。16S rRNA基因由高度保守的核苷酸序列和具有属或种特异性的可变区域组成。研究人员找到保守区域,然后放大并分析散布的可变区域——将它们与参考序列进行比较,以确定存在的细菌种类。
然而,鉴于每个基因组只有一个基因被检查,所以16S测序只能提供非常有限的关于微生物群落功能潜力的信息。它低估了样品中微生物的总多样性,不能轻易区分亲缘关系密切的细菌,也不能检测到其它微生物,如真菌和病毒——这些微生物也有助于微生物组功能。
测序成本的下降和改进计算方法的发展导致了“鸟枪法宏基因组学”(shotgun metagenomics)的广泛采用。使用这种方法,研究人员可以通过对提取的DNA片段进行测序,然后将它们与参考数据库进行比较,或者根据重叠序列的相似性对其进行组合,从而分析样本的整个基因组内容。利用鸟枪法宏基因组学,研究人员可以识别基因或基因片段,并预测其编码蛋白的功能。虽然这是一项强大的技术(提供了微生物群落功能潜力的信息),但由于序列读取不局限于单个位点,如16S rRNA基因,所以需要更深入的测序,以实现类似的检出率。这可能使鸟枪法宏基因组学在大规模研究中昂贵得令人望而却步。
然而,研究人员正越来越多地转向鸟枪法宏基因组学。Schroth指出,与16S测序相比,鸟枪法宏基因组学提供了更丰富的信息。通过调整测序深度,可以在不影响结果的情况下控制成本。
浅层测序依赖于微生物参考基因组重组片段,这限制了它的应用。对于绝大多数微生物来说,这些还不存在。Bhatt表示,我们主要在一个没有参考的空间里工作,无法绘制很多我们生成的参考基因组的片段,开发新的检测基因组的方法是一个令人兴奋的挑战,而且可以从深度的全元基因组测序中获益。
功能性生物勘探
最终,为了了解肠道微生物群落的功能,有必要确定哪些基因被表达,并被翻译成蛋白质。因此,科学家用元基因组数据对RNA测序数据进行补充,而RNA测序可与元转录分析和分子分离方法并行,最后结合质谱或核磁共振来构建组成群体的元蛋白质组和元代谢组谱。
波士顿哈佛大学公共卫生学院(Harvard T.H. Chan School of Public Health)的计算微生物学家Curtis Huttenhower指出,越来越多的研究人员单独使用鸟枪法宏基因组学,或者与其他方法(如群体代谢组学)结合使用,将测序与高通量分子工具联系起来,让我们能够以新的方式观察微生物群落。元代谢组学分析可以通过识别肠道微生物代谢与心血管疾病风险或胰岛素敏感性之间的联系机制,来帮助验证元基因组的发现。
Hutenhower还是人类微生物组生物活性资源(Human Microbiome Bioactives Resource,HMBR)的首席研究员,该机构提供平台和方法,结合16S测序、鸟枪法宏基因组学、元转录组学和元代谢组学,以鉴定微生物组。HMBR的目标是识别对人类疾病有重要影响的微生物产品,并确定其功能。Hutenhower提醒,我们正在研究数量惊人的、与疾病表型有关,并受免疫活动或饮食调节的未鉴定基因、基因产物和代谢物。事实上,人类肠道微生物组中超过50%的基因还没有被鉴定出来。我们还需要一段时间才能实现这个目标。
学会操纵肠道微生物群
在过去的十年中,临床医生已经能够通过粪便移植将“坏”的微生物群替换为“好”的微生物群,从而改变病人的微生物生态。这些药物似乎对某些疾病有效,特别是反复发作的艰难梭状芽胞杆菌(Clostridium difficile)感染,但对其它胃肠道疾病的疗效仍存在担忧。
撇开肠胃疾病不说,关于微生物群的作用以及它可能受到的影响,我们了解得更少。在接受造血干细胞移植的癌症患者中,某些肠道细菌与移植后感染有关。Bhatt指出,在接受干细胞移植的患者中,约40%出现了血流感染,我们可以将引起感染的病原体追溯到肠道微生物群。
此外,当来自供者移植的免疫细胞攻击接受者的组织时,移植物抗宿主病的发生率和严重程度与肠道微生物群的变化有关,包括微生物的多样性。拥有不同肠道微生物类型的生态系统有助于调节宿主炎症和免疫耐受。Bhatt的团队目前正在研究粪便移植和益生元是如何改变干细胞移植患者体内的微生物群组成,并改善他们的预后的。
也许还有其它不需要替换整个微生物组的治疗方法。去年,Bhatt等人的报告指出,存在着成千上万种曾被忽视的小蛋白质(长度少于50个氨基酸),它们可能在微生物与其它微生物以及宿主细胞的通讯中扮演重要角色。对这些蛋白作用的进一步了解可能会导致更有针对性和更有效的治疗方法。
Huttenhower的团队还对肠道生态系统中的特定成分感兴趣,无论是在人体细胞还是在微生物中,这需要详细的功能理解。他表示,他们希望能设计出针对正确宿主免疫受体的小分子,或者能够抑制或激活正确的微生物代谢途径,以解决特定问题。
作为他们研究IBD(包括克罗恩病和溃疡性结肠炎)工作的一部分,他们已经能够通过计算预测胆汁酸和微生物蛋白在肠道炎症中的作用。通过使用微生物和哺乳动物细胞,以及体内微生物全部已知或不存在的无菌小鼠来测试作用机制,科学家可以在受控的实验设置中确认预测的生物活性,并评估这些生物活性化合物对IBD致病性的贡献。
前景和挑战
为了改进肠道微生物的功能分析,并开发有针对性的方法来调节它,Bhatt强调需要在不同的时间点收集和对样本进行测序。她提醒,微生物是不稳定的,也不会静止不动,它们是活体,在不同的临床环境中具有选择性优势。Bhatt期待进一步的技术发展,以帮助更准确地检查一个群落内的微生物基因组如何随时间变化。
当涉及到检测微生物之间的基因交换(水平基因转移(horizontal gene transfers))时,目前的方法也很糟糕。水平基因转移是微生物适应不同环境的关键因素,例如抗生素的存在。Bhatt的团队正在探索解决这一检测问题的方法,通过对更长的DNA片段进行测序,使其更容易比对,从而实现更精确的细菌基因组组装。
二代测序技术已经改变了宏基因组学领域,这一点毫无疑问。分析方法的进一步发展,包括机器学习,将多组微生物组数据整合起来,将对人类疾病产生深远影响。Huttenhower指出,随着检测和分析微生物的工具数量的增加,可以提出的问题的多样性和潜在的转化应用的数量也在增加。
原文检索:
https://www.nature.com/articles/d42473-020-00214-9
张洁/编译

的来源,而测序正在揭示它的秘密。-300x241.jpg)