抗体成像助力癌症研究
使用抗体的正电子发射断层扫描(Positron-emission tomography, PET)成像可以帮助研究人员观察小鼠和其它动物体内潜在的癌症位置。
新技术帮助研究者深入理解免疫系统的作用机制。
抗癌药物的研发过程非常曲折:起初,细胞实验和小鼠实验的前景都非常乐观;但是,随后的猴子试验就非常让人沮丧:猴子们被那些旨在靶向和杀死胰腺癌细胞的药物毒死了。
该药物的研发团队成员、加州Genentech公司的Simon Williams指出,团队检验过收集的组织样本,但是没有发现任何迹象提示药物具有毒性。当研究人员对活体进行成像,并跟踪药物在动物体内的扩散时,他们终于找到了症结所在:这种基于抗体的药物主要被动物的骨髓吸收,进而杀死骨骼的白细胞。鉴于此,研究人员放弃了这种药物。
当生物药物进入活体时,研究人员往往不知道后续会发生什么情况。从早期试验到最终应用于临床,他们并不能确定药效究竟如何。有时患者会对药物产生响应;有时则不会。无论结果如何,研究人员都想知道为什么。但通常他们缺乏合适的研究工具。
现在,成像科学家和癌症研究人员正在试图解决这个问题。他们将传统PET(Positron-emission tomography,正电子发射断层扫描)技术与抗体和类似分子结合起来,创造了一种名为immunoPET的新技术。研究人员表示,随着癌症治疗变得越来越精确和复杂,用于评估疗效的工具也需要不断改进。现代生物治疗只适用于部分患者,但是医生还不能可靠地预测哪一部分患者适用于这种治疗。活检只能告诉你一个肿瘤的一部分发生了什么,immunoPET则可以提供身体里所有肿瘤的快照。
传统PET使用放射性示踪剂来观察人体组织功能,而immunoPET则则使用抗体来识别目标细胞。随着癌症免疫治疗的蓬勃发展和调动免疫系统来对抗肿瘤的治疗策略的越来越流行,癌症领域对这种新兴成像技术兴趣大增。但是设计immunoPET成像探针并不容易。放射性示踪剂的选择、抗体设计和成像动力学等因素都需要审慎考虑。不过幸运的是,目前科学家们已经取得了一些进展。现在,他们可以鉴定越来越多的免疫细胞和癌症组织,并且正在调整抗体结构以改善其性质。新的治疗和成像策略呼之欲出。
斯坦福大学(Stanford University)放射科主任、致力于癌症早期检测和管理的分子成像研究者Sam Gambhir指出,这种“免疫工具箱”非常必要。他们做的大多数治疗干预措施都是盲目射击,不知道治疗是否有效,特别是早期阶段。人们只能看到肿瘤是否真的缩小了?但如果不缩小,就不知道哪里出了问题。这意味着,人们可能不知道下一步该怎么做。
潜力无限的PET
狭义来说,immunoPET是使用抗体或相关分子作为成像剂的工具。研究人员选择一种抗体或类似分子来识别感兴趣的细胞——例如帮助癌症细胞免受免疫系统攻击的PD-L1,或标记杀伤T细胞的CD8。把抗体注射到动物体内,抗体就会扩散到身体各处,直到到达靶细胞并与其结合。
为了“看到”这些细胞,研究人员用半衰期较短的放射性同位素(通常为锆-89或碘-124,半衰期分别为3.27和4.18天)标记抗体。这些PET标签发射正电子——电子的反物质。当正电子与身体中的电子碰撞时,会产生一对γ射线颗粒,彼此反向高速离开。只要同时检测这一对粒子,就可以显示体内目标物的位置和丰度了。研究人员可以将这些数据叠加到计算机断层扫描(computed-tomography, CT)或磁共振成像扫描()magnetic resonance imaging scans, MRI scans)图像中,以确定抗体标签的解剖位置。
生物学家和临床医生正在使用immunoPET来解释为什么一些患者对治疗产生响应,而其他患者则没法响应。
例如,几年前,荷兰格罗宁根大学医学中心(University Medical Center Groningen)的医学肿瘤学家Elisabeth de Vries等人对56名晚期乳腺癌患者进行了immunoPET成像。该组患者接受了trastuzumab emtansine(Kadcyla)药物治疗。Kadcyla是一种偶联药物,它由与肿瘤蛋白HER2结合的抗癌抗体trastuzumab与靶向目标细胞的化疗药物结合而成。通过使用放射性标记,该小组发现,29%的患者的肿瘤没有大量吸收抗体。这意味着患者不太可能从治疗中受益;实际上,该组患者的生存期中位数为2.8个月,最后试验以失败告终。而那些肿瘤摄取较多抗体的患者的生存期中位数为15个月。De Vries等人和荷兰三家研究机构正在进行一项试验,以测试这种前期成像是否能改善200名新诊断为转移性乳腺癌女性患者的治疗方案。该试验预计在今年晚些时候完成志愿者招募工作。
在另一项研究中,de Vries等人证实,当癌症已经损害血脑屏障时,抗体可以达到神经胶质瘤。这表明,与常规观念相反,基于抗体的治疗可能可以有效对抗神经胶质瘤。 de Vries指出,传统理论认为,抗体分子太大了,以致无法穿过血脑屏障,然而事实并非如此。
许多癌症发展迅速,当它们传播或转移到身体的其它部位时,它们可能与原始肿瘤不同。因此仅仅对一个转移肿瘤进行活检是不够的。ImmunoPET扫描全身的能力也有助于解决这个问题。纽约市纪念斯隆凯特琳癌症中心分子成像和纳米技术中心(Center for Molecular Imaging and Nanotechnology at Memorial Sloan Kettering Cancer Center)主任Jason Lewis表示,癌症患者的转移灶往往不止一个,可能有多个,但你无法对这些转移进行一一活检。不过现在有了immunoPET,研究者和医生就可以对这些转移灶进行成像了。在一项2016年开展的immunoPET研究中,Lewis等人确定了两名HER2阳性转移的女性,她们的原发性肿瘤为HER2阴性;这两名患者对曲妥珠单抗治疗有响应。
辅助免疫治疗
加州大学(University of California)洛杉矶分校的医学肿瘤学家、黑色素瘤研究者Antoni Ribas指出,正在开发的免疫治疗也可能受益于immunoPET。例如,在免疫检查点抑制疗法中,肿瘤细胞表面的一个受体与T细胞表面的一个受体相互反应,从而抑制T细胞的免疫功能。免疫检查点抑制剂与这两个受体中的一个结合,并抑制其活性,从而激活肿瘤周围的T细胞,使其行使肿瘤杀伤功能。
但是,Ribas表示,这种杀伤机制的一个基本假设是通过细胞表面蛋白CD8可以识别那些位于肿瘤附近的杀伤性T细胞。但事实并非如此。使用immunoPET,你可以确定免疫系统是否可以激活,如果肿瘤处没有CD8细胞存在,那么使用检查点抑制剂并不能激活该处的T细胞。这类患者将需要其它治疗方案。
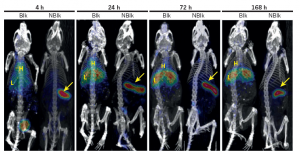
小鼠注射PET示踪剂后不同时间点的PET与CT叠加图像。BLK:空白对照组;NBLK:实验组。
Ribas指出,当免疫细胞过度激活,损伤其它组织时,免疫检查点治疗可能会引起令人讨厌的副作用。例如,肠道炎症是黑素瘤检查点抑制剂药物ipilimumab(Yervoy)的常见副作用。他推测,也许immunoPET可以让临床医生尽早观察到这些副作用的蛛丝马迹。
诸如此类的临床问题使得Ribas与加州大学洛杉矶分校(University of California, Los Angeles)成像科学家Anna Wu(加州成像公司ImaginAb的联合创始人,目前从事改进抗体,优化immunoPET的工作)合作。2015年,Wu的团队与Ribas等人使用immunoPET跟踪三种免疫疗法实验中小鼠体内的杀伤T细胞。放射性标记探针——靶向CD8受体的抗体片段显示T细胞聚集在肿瘤中,并改变肿瘤在身体其它部位的分布。
Wu指出,ImmunoPET甚至可以在治疗早期,在肿瘤开始缩小之前揭示治疗是否有效。事实上,初始治疗后,肿瘤可能没有缩小,反而会变大——免疫细胞浸润肿瘤,使组织发生肿胀时,研究人员和临床医生有时会误以为治疗无效。ImmunoPET可以揭示细胞类型之间的差异,并在肿瘤细胞明显开始死亡之前显示治疗有效。
Williams表示,在药物开发实验室,immunoPET可以帮助研究人员决定是否应该继续研发一个抗体。在临床前工作中,immunoPET证实了一种名为STEAP1的抗体的潜力。该抗体靶向转移性前列腺癌细胞,其连接的药物会杀伤癌细胞。在早期(未发表)临床试验中,成像显示抗体组分甚至可以到达曾被认为是不可接近的组织中的转移瘤,例如骨骼。以前免疫治疗领域一个经常讨论的问题是:抗体能否转运到骨转移瘤?成像结果给了我们肯定的答案。
Williams的immunoPET有助于研究本文开头提到的抗体—药物偶联物在非人灵长类动物上的重大毒副作用的案例,以查明为什么那种药物如此致命。
快速递送
研究人员指出,单克隆抗体能够产生非常漂亮的immunoPET图像。但是,将抗体送至目标的组织,并将未与靶细胞结合的单抗排出体外,从而产生良好的对比度和特异性的图像的整个过程可能需时一周。
一些情况下,这个时间尺度是可以接受的。例如,在药物开发方面,研究人员需要就是否继续开发候选药物做出决定,一般没有时间去等待新的、更快速的成像剂问世。Williams指出,管理层必须决定:我们要继续临床3期试验吗?如果成像不能在限定时间里做出,就毫无意义。
但在临床方面,时间是成像测试的首要考虑因素。约翰霍普金斯大学(Johns Hopkins University)分子成像科学家Sridhar Nimmagadda表示,一般immunoPET用于晚期癌症患者,这些患者常常有转移。对于这样病情严重的病人来说,临床决策需要尽快做出,一周还是太长了。
因此,研究人员也在努力开发精度不低于抗体,但分子量更小,药代动力学更理想的分子。例如,Wu的实验室已经设计了名为“微型抗体”和“双抗体”的细长抗体变体。这些抗体保留了传统单抗与抗原相互作用的部分(称为可变结构域),但是去除了与免疫系统其它部分(例如清除细菌和碎片的细胞)接触的部分。所这些抗体只保留了与目标分子结合的能力。Wu指出,病人注射这种抗体后,一天内就可以成像。
Wu还表示,这些蛋白质变体还有其它有用的特性。例如,它们能否通过肝脏或肾脏排出体外,这取决于它们的大小。为了提高对比度,并获得盆腔肿瘤的清晰形象,临床医生将选择通过肝脏清除的抗体;对于胰腺癌,通过肾脏清除的抗体则会更合适。Wu还可以改变这些工程化的抗体片段,使其尽可能地贴近人的内源性蛋白,减少造成的免疫排斥反应(因为它们不是天然的人类蛋白质),或者使放射性同位素标记物以统一的方式附着于蛋白质上,这有助于确保抗体活力的一致和可靠性。Wu指出,这就是蛋白质工程师的任务了。只要你想生产重组蛋白质,你就可以你能优化的蛋白的一切特性。
其他实验室,如波士顿儿童医院(Boston Children's Hospital)分子生物学家Hidde Ploegh的实验室,利用美洲驼、羊驼和骆驼的抗体获得了药代动力学更快的immunoPET成像剂。这些骆驼种类产生的抗体仅含有一种类型的链,而不是常规抗体那样,由两种链组成,其重量仅为常规抗体的十分之一。但它们也比常规抗体更易被清除,并且在组织中的浸透深度更深。
放射学家和分子成像科学家Martin Pomper指出,任何允许病人在几小时内成像,然后离开医院的方法都是值得鼓励的。Pomper是约翰霍普金斯大学(Johns Hopkins University)核医学和分子成像系的主任,Nimmagadda就职于该院系。
但是Pomper和Nimmagadda认为,临床的最佳方法不在于抗体或抗体变体,而是更小的肽和其它低分子量分子。该团队开发了一种放射性标记的肽,这种肽能与PD-L1结合,并可以在两小时内成像。目前该小组还在研发更小的成像剂。
标签两步法
保持抗体精确度的另一个策略是采取两步法。研究人员往病人体内注入抗体,然后等待一周,等不与靶标结合的抗体排出体外。接着注射第二个较小的标记探针,其迅速与第一次注射的抗体结合。这种方法中使用的放射性同位素半衰期更短,例如可以采用半衰期分别小于2小时和12.7小时的氟-18或铜-64。
该方法取决于“双特异性”抗体的产生。这种抗体具有两个结合位点——一个位点与蛋白质靶标(如PD-L1)结合,另一个位点与放射性标记探针结合。
纪念斯隆-凯特琳癌症中心(Memorial Sloan-Kettering Cancer Center)分子药理学项目主管Steven Larson指出,与immunoPET一样,两步策略并不是什么新想法。但是,现在成像和抗体工程的进步让两步策略成为了一个令人兴奋的产物。Larson相信,这种方法可以为放射免疫疗法(利用抗体特异性,靶向性地向肿瘤递送放射性毒性药物)这种旧治疗策略注入新活力。Larson表示,现代成像使医师能够精确地校准剂量,避免损伤正常组织。
他还补充,如果实质瘤没有在早期被发现,那么患者就很难完全治愈。他们想通过这种方式根治癌症,并且认为可行性很高。
Gambhir表示,开发和测试癌症疗法的研究人员通常没有意识到成像技术是非常实用的工具。但他们正在学习。1月份发表的一篇论文显示,在免疫治疗试验中,工程化的T细胞到达胶质瘤后,可以被PET成像剂跟踪。这篇文章发表后,他收到了很多来自业界的咨询。制药公司的电话Gambhir已接到手软。药企一看到人体上的试验结果,就兴奋起来了。
原文检索:
Rosie Mestel. (2017) Cancer: Imaging with antibodies. Nature, 543(1038): 743-746.
张洁/编译