COVID-19疫苗研发获得了生物技术的推动
北京科兴生物制品有限公司(SINOVAC BIOTECH CO., LTD.)的研究人员正在研发SARS-CoV-2疫苗。
疫苗技术的进步正在加速遏制冠状病毒以及其它病原体的传播。
1月,Barney Graham研发的一种新型疫苗即将进行测试,此种疫苗靶向尼帕病毒(Nipah virus),这种病毒在过去东南亚爆发的疫情中曾引起呼吸道疾病和脑部感染。Graham是一位疫苗学家,同时也是位于马里兰州贝塞斯达的美国国家过敏和传染病研究所(US National Institute of Allergy and Infectious Diseases, NIAID)疫苗研究中心的副主任。他正在与马萨诸塞州剑桥市的Moderna Therapeutics公司合作,制造一种以往从未被批准使用的疫苗。与大多数疫苗基于完整的病原体或其结构成分不同,Moderna的疫苗是由病原体的RNA构建的。该团队希望接种者的细胞能利用RNA制造蛋白质,启动免疫系统从而产生保护性应答。
Graham等人刚着手制造用于人体试验的尼帕疫苗(Nipah vaccine),就收到了由一种新的冠状病毒(现在称为SARS-CoV-2)引起的疾病在中国武汉肆虐的消息。他们很快改变了研究计划,但没有改变疫苗的设计原理。当1月11日网上共享了SARS-CoV-2基因组序列的草图后,Moderna转而研究冠状病毒RNA,并开始将一批有潜力的疫苗运送到NIAID进行临床测试。这一过程仅用了6周,这是医学史上从项目启动到开始候选疫苗最快的周转时间。
Graham的团队是150多个疫苗研发团队中的一员,他们正在争分夺秒地研发疫苗,以降低COVID-19的严重程度,或者说阻断SARS-CoV-2的感染。得益于新兴疫苗技术的浪潮,这些科学家比以往任何一种新病毒都有更大的成功机会。费城宾夕法尼亚大学(University of Pennsylvania)的免疫学家Drew Weissman表示,真正的挑战是速度。但是,无论疫苗是否能保护人类免受疾病感染,都不应该以牺牲安全性或疗效为代价。
如今,RNA疫苗等方法正在帮助研究人员以最快的速度开发和测试候选疫苗。NIAID主编Anthony Fauci在6月23日对美国国会委员会声称,他对2021年初将产生有效的疫苗持“谨慎乐观”的态度。与《自然》(Nature)杂志交流的疫苗学家也有同感。尽管他们认为,第一批疫苗可能不是最好的设计,改进后的版本可能会在随后出现。许多已经在开发的疫苗都有可能成为那些二代疫苗。有几个小组正在应用结构和计算机分析免疫系统与病毒抗原(病毒中引发免疫反应的部分)之间的相互作用进行研究。这些技术已经针对许多病原体进行了尝试,目前正在应用于SARS-CoV-2。
蓄势待发
这是疫苗专家一直在准备的时刻。在2014-2016年西非埃博拉病毒(Ebola viruses)大面积爆发后,世界卫生组织(World Health Organization, WHO)公布了一份被认为最有可能在未来导致严重疾病爆发的病原体短名单(go.nature.com/2deknbt)。其中包括引起严重急性呼吸道综合征的冠状病毒(SARS-CoV)、引起中东呼吸道综合征的相关冠状病毒MERS-CoV以及一些尚未知晓,但存在威胁的病毒。2017年“流行病防备创新联盟”(Coalition for Epidemic Preparedness Innovations, CEPI)发起了一项全球性的项目,旨在联合公共、私营、慈善和民间社会组织,开发疫苗以预防未来流行病的爆发。
虽然SARS-CoV-2是一种新病毒,但研究人员已经对冠状病毒的一般特点有了诸多了解,并从2003年的SARS和2012年的MERS爆发期间开始的疫苗研究中获得了很多经验。一个很有前景的SARS-CoV-2疫苗的候选抗原被称为刺突蛋白(spike protein),它从病毒中伸展出来,形成“皇冠”的外形,这就是冠状病毒名称的由来。刺突蛋白附着在细胞上,为病毒入侵细胞提供入口。与刺突蛋白结合的抗体可阻止病毒进入细胞,因此阻断病毒感染。这种中和抗体(neutralizing antibody)是许多疫苗的目标。此外,能够诱导产生T细胞的疫苗也是可取的,因为T细胞是产生全面免疫反应所需的一种免疫细胞。
推动这些成果的是大量公共和私人资金的注入。据CEPI估计,该公司与总部位于伦敦的制药巨头GlaxoSmithKline公司合作开发的疫苗将耗资20亿美元,并且该公司已经筹集了超过一半的资金。CEPI还向其他合作伙伴投资了数亿美元,包括英国剑桥的AstraZeneca公司和马里兰州盖瑟斯堡的Novavax公司。美国生物医学高级研究与发展局(US Biomedical Advanced Research and Development Authority)已经向Moderna、Merck、Janssen、AstraZeneca和Novavax在内的公司投入了约38亿美元用于疫苗开发。
这些钱用于开发疫苗并将其投入临床试验,以及制造充足的成功疫苗加以使用。位于宾夕法尼亚州斯威夫特沃特的Sanofi Pasteur公司的疫苗研发负责人John Shiver表示,证明它有效是一方面,能够充分供给又是另一方面。赛诺菲计划(Sanofi plans)重新利用其只在季节性所需的流感疫苗设施,生产其正在开发的基于蛋白质的SARS-CoV-2疫苗。其他公司仍在钻研如何安全地大规模生产新型疫苗,如含有RNA的疫苗。
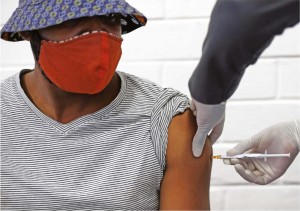
南非索韦托的一名志愿者在临床试验中注射SARS-CoV-2疫苗。
加快研制速度
早期的抗病毒疫苗是由减毒、灭活或存活但无害的病原体制成的生物制剂。这些方法至今仍在使用,使用分离的蛋白质或碳水化合物作为抗原的方式也是如此。
对于这些种类的疫苗,研究人员或多或少都要为每一种新的病原体重新制定计划。相比之下,许多正在开发的疫苗依赖于“平台技术”(platform technologies),基本上是“即插即用”(plug-and-play)。对于这些,研究人员确定他们认为可能是有效的抗原,并将其DNA或RNA序列置于预先验证的平台(例如另一个病毒基因组或一部分DNA或RNA),以快速创建一个候选疫苗。英国牛津大学(University of Oxford)的疫苗学家Sarah Gilbert表示,这对于新发病原体疫苗的开发是非常理想的。然而,由于技术相对较新,这些平台还没有生产人类使用疫苗产品的许可,只有少数基于DNA的兽医用疫苗,例如用于马西尼罗河病毒(Nile virus)的预防。班加罗尔印度科学研究所(Indian Institute of Science)的病毒学家Shashank Tripathi认为,平台技术还没有真正大规模地进入人们的视野。COVID-19可为平台的初次亮相提供机会,为针对其他人类疾病的平台疫苗奠定基础。
Moderna的疫苗是基于信使RNA(messenger RNAs, mRNA),用于指导细胞生成蛋白质抗原。他们的设想是,一旦一个人收到注射疫苗中的这些mRNA的指令,被注射者的细胞就会开始产生蛋白质。然后,这些蛋白质会出现在细胞表面或被释放到血液循环中,从而吸引免疫系统的注意。
Weissman是共同开发Moderna疫苗应用技术的研究者,他已经建立了针对流感病毒、单纯疱疹病毒2(HSV-2)和HIV的候选RNA疫苗,并预计在一年内启动这些疫苗的人体试验。在动物研究中,他的团队针对HSV-2的RNA疫苗表现优于基于蛋白质的疫苗。Weissman表示,当他们使用RNA时,它的效果更好。部分原因可能是RNA在细胞中可以持续存在约两周,这给免疫系统检测抗原和建立免疫力提供了时间。
在1期安全试验中,人们很好地耐受了Moderna的SARS-CoV-2的mRNA疫苗,2期研究已经开始确定所需剂量。一项旨在评估疫苗疗效的3期试验计划于本月开始。
然而,尽管该技术看似简单,但却给疫苗开发者带来了新的挑战,例如如何制造大量的医疗级别RNA。位于德国图宾根的CureVac公司也在开发RNA疫苗,该公司首席技术官Mariola Fotin-Mleczek表示,该公司已经研究出如何做到这一点。RNA天然不稳定,需要在零下20℃以下冷冻保存,这将使RNA疫苗的运输和临床应用变得复杂。但CureVac和其他公司正致力于在高温下稳定分子,例如通过冷冻干燥技术。
费城威斯达研究所(Wistar Institute)执行副所长、分子免疫学家David Weiner表示,DNA更稳定,它在室温下可以保存一年,在冰箱里可以保存更长时间,Weiner正在开发DNA疫苗。这些疫苗的工作原理与RNA疫苗相同,疫苗的DNA编码一种蛋白质抗原。当进入细胞时,DNA被转录成mRNA,提供制造病毒蛋白的指令。Weiner已经在人们身上测试了DNA疫苗,以预防HIV、埃博拉、MERS和寨卡病毒(Zika viruses)。他的寨卡疫苗,从开始研究到人体测试只用了6.5个月,保持了记录以来最快的疫苗研发速度。
在宾夕法尼亚州普利茅斯会议(Plymouth Meeting)中,Inovio制药公司已授权Weiner的技术,6月30日报告称,其基于DNA的SARS-CoV-2疫苗在1期人群试验中是安全的(go.nature.com/3jeyjyd)。此外,大多数参与者都建立了由抗体和T细胞组成的免疫反应,计划在今年晚些时候进行2期/3期试验以测试疫苗的剂量和疗效。
Weiner表示,得益于已有的基因疗法、制造大量特定DNA片段的技术已经可行。兽用DNA疫苗和一种针对人类乳头瘤病毒的免疫疗法目前正在进行3期临床试验。DNA疫苗的挑战在于传递,遗传物质必须穿过细胞膜并进入细胞核。通常,皮肤的电脉冲被用于打开细胞膜。Weiner表示,这并不像听起来那么不愉快,它的耐受性很好。
在牛津大学,Gilbert有其自己的疫苗平台,名为ChAdOx1,它基于黑猩猩腺病毒。利用腺病毒(adenovirus)基因组作为载体,牛津大学团队添加了编码抗原的DNA序列(对于SARS-CoV-2来说,就是刺突蛋白),并将产生的病毒颗粒注射到受试者体内。腺病毒唤醒了免疫系统,被感染的细胞在其表面显示出刺突蛋白。由于这种腺病毒不会复制,所以需要进行高剂量注射,随着免疫系统的启动,会产生大约12小时的流感样症状。但任何受感染的细胞最终都会被免疫细胞吞噬,所以它是完全安全的。相关疫苗如以泡性口炎病毒(vesicular stomatitis virus)为载体的一种抗埃博拉病毒的疫苗,病毒可以自我复制,这增加了因载体而产生副作用或疾病的风险。
牛津大学小组已经在小规模的人体试验中测试了针对MERS、流感和肺结核的ChAdOx1疫苗,并正在与AstraZeneca公司合作生产一种针对SARS-CoV-2的疫苗。该疫苗已经进入2期/3期试验,这将确定它是否能保护人们免受疾病侵害,以及是一剂还是两剂更有效。
更智慧的研发
随着第一代SARS-CoV-2疫苗进入临床试验阶段,研究人员正在努力开发第二代疫苗,将他们从其它病毒疫苗开发中获得的所有经验融入其中。
例如,HIV病毒不断变异,使得免疫系统很难形成能够阻止所有不同版本病毒的广泛的中和抗体。在一项被称为“抗体组学”(antibodyomics)的技术中,研究人员应用信息学分析了广义中和抗体的特征和发展,有望设计出更有效的疫苗。
在抗原方面,巴西的研究人员开发了一种他们称之为“免疫信息学”(immunoinformatics)的方法来识别潜在的候选疫苗。欧陆普雷图联邦大学(University of Ouro Preto)的寄生虫学家Alex Reis和其验室的免疫寄生虫学家Rory Brito博士后将该技术应用于内脏利什曼病(visceral leishmaniasis)疫苗的研究,这种疾病是由原生动物寄生虫—利什曼原虫(Leishmania)引起的,它能使人和犬类感染,特别是多发于南美洲和地中海地区。
Reis已经开发出一种基于破碎的寄生虫细胞的利什曼病候选疫苗,目前正在进入3期试验。但其生产需要种植大量的寄生虫,他认为可以利用利什曼病抗原中的单个多肽研发出更有效的疫苗。
Reis和Brito想通过刺激T细胞来对抗病原体。首先,Brito培训计算机算法来识别寄生虫抗原中被预测为最能刺激T细胞反应的肽段。然后,利用计算分析和动物研究,他将寄生虫的8,000多种蛋白质缩小到4种他预测可能有效的肽段。小鼠体内注射了这4种肽段,随后又注射了利什曼寄生虫,与未接种疫苗的动物相比,混合肽段激活了T细胞免疫,减少了寄生虫的数量。但是Reis和Brito还没有将免疫信息学候选疫苗与Reis的原始利什曼病疫苗进行比较。
Brito表示,使用信息学,可以在短时间内提出候选疫苗,并且成本应该会更低。他补充到,免疫信息学应该适用于任何病原体。Reis和Brito正在申请资金,用于在SARS-CoV-2上尝试他们的方法。他们希望确定病毒抗原,也许并不是刺突蛋白的抗原,可以产生对SARS-CoV-2和其它冠状病毒的免疫力。
同样影响疫苗开发的还有对病原体蛋白结构的研究。例如,Graham和他的合作者已经将基于结构的设计应用于呼吸道合胞病毒(RSV),该病毒可引起婴儿和老年人的严重气道和肺部感染。几十年来,此病毒一直对尝试阻止它的疫苗产生抵抗。
RSV的中和抗体往往与病原体用于进入细胞的病毒蛋白融合前的变体结合。2013年,该团队确定了该预融合变体与中和抗体复合物结合的结构。然后,研究人员对其氨基酸进行了改造,将其固定于该形状。他们推断,由该病毒结构制成的疫苗将更有可能产生这种抗体。在一项人体试验中,Graham的疫苗比其它RSV疫苗更能提高血液中的中和抗体活性,甚至比病毒本身更强。
研究人员现在正将同样的方法应用于SARS-CoV-2,使用稳定的刺突蛋白结构,希望创造出更强效的疫苗。
Graham认为,病原体结构可能会成为未来每一个疫苗开发程序的一部分。
跃过终点线
随着COVID-19疫苗的蔓延,下一个障碍是测试。从临床前研究到投入生产可能需要十年甚至更长时间。目前感染人数和死亡人数都非常多,而且数量还在不断增加,世界已经等不及了。但是,正如研究人员在埃博拉病毒爆发期间所了解到的那样,平行运行不同阶段的疫苗研究和测试,而不是采取传统的按部就班的方法,可以加快开发速度。新西兰奥克兰大学的疫苗学家Helen Petousis-Harris表示,这些研究上的挑战已经在某种程度上被击溃了。
此外,疫苗学家计划通过在SARS-CoV-2传播迅速的热点地区的大批人群上运行试验来加速疫苗测试。Weissman表示,这样一来,疫苗组和安慰剂组之间任何感染率的差异应该都会很快出现。
据该公司报道,由中国天津的CANSINO生物公司制造的一种基于腺病毒平台的疫苗于6月25日被中国军方批准为“特需药”,此前未公布的2期试验结果表明,该疫苗具有预防SARS-CoV-2引起的疾病的潜力。
一旦科学家找到了一种有效的疫苗,挑战就会转移到制造上。Fotin-Mleczek表示,他们正在谈论需要数十亿的疫苗,这真的很困难。她指出,可能也需要类似数量的无菌针头和其他设备。
药品制造商现在正在制造疫苗,希望一旦知道它们有效,就能广泛分发。Petousis-Harris认为,投资回报没有保证,但如果一种疫苗有效,就拥有了领先地位。
到明年,疫苗学家希望不仅得到有效的COVID-19疫苗,而且能了解一系列关于其开发的新经验。Gilbert表示,将这些齐头并进的技术相互比较将会非常有趣,他们将在下一次流行病中处于一个更领先的位置。
原文检索:
Janice Hernandez. (2020) Coronavirus vaccines get a biotech boost. Nature, 583: 647-649. 郭庭玥/编译

的研究人员正在研发SARS-CoV-2疫苗。-300x295.jpg)