SARS-CoV-2研究进展神速
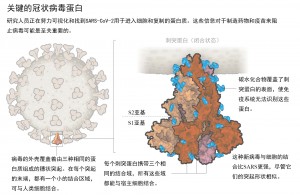
阻止新冠病毒疫情,可能依赖于对SARS-CoV-2蛋白的可视化研究,并利用它们设计药物和疫苗。
1月10日晚上,躺在床上用智能手机浏览新闻的Andrew Mesecar收到了一条警报。他坐了起来。冠状病毒又来了。在中国武汉,一种引起肺炎样病例的冠状病毒的完整基因组刚刚在网上公布。
在世界各地,类似的通知出现在科学家的设备上,他们在2003年SARS(severe acute respiratory syndrome,严重急性呼吸综合征)爆发时首次与冠状病毒交锋,然后在2012年再次与MERS(Middle East respiratory syndrome,中东呼吸综合征)交战。研究人员立即动员起来对付一个新的对手。印第安纳州西拉法叶普渡大学(Purdue University)生物化学主任Mesecar指出,他们一直都知道它会回来,这是历史告诉他们的。
在德国吕贝克,Rolf Hilgenfeld停止了退休前的打包工作,开始为晶体学研究准备缓冲液。在明尼苏达州,Fang Li彻夜未眠,分析新的基因组并起草一份手稿。在中国上海,杨海涛召集了12名研究生,让他们腾出时间。在德克萨斯州,Jason McLellan指导实验室成员开始从病毒基因组中组装基因序列。
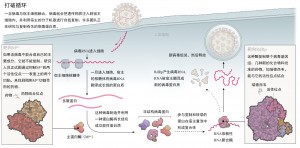
在24小时内,世界各地的一个结构生物学家网络将他们的实验室重新定向到一个单一目标——解决一种致命的、迅速蔓延的新传染病的蛋白质结构。要做到这一点,他们需要对病毒基因组中的29811个RNA碱基进行筛选,找出其25-29种蛋白质的每一种的指令。有了这些指令在手,科学家就可以在实验室里重现这些蛋白质,将它们可视化,然后,有可能识别出药物化合物来阻止它们,或者开发出疫苗来刺激免疫系统对抗它们。
1月11日:全球41例新冠肺炎确诊病例
第二天早上6点,Mesecar醒来,打开咖啡壶,开始在新的基因组中寻找可识别的蛋白质序列。这没花多长时间,毕竟他花了17年来研究冠状病毒,这种新病毒的基因组看起来非常熟悉。Mesecar认为,这和SARS是一样的。
Mesecar立刻联系了伊利诺伊州芝加哥西北大学芬伯格医学院(Northwestern University Feinberg School of Medicine)的微生物学家Karla Satchell。Satchell是传染病结构基因组学中心(Center for Structural Genomics of Infectious Diseases, CSGID)的联席主任,这是一个由8家机构组成的联盟,专门为类似时刻而成立,目的是快速研究新出现的传染病病原体的结构。
为了在高分辨率下解决蛋白质的3D结构,科学家首先设计了一个基因结构——一个包含蛋白质指令的DNA环,以及控制蛋白质表达的位置和方式的调控序列。然后,他们将构建物插入活细胞(通常是大肠杆菌),利用细胞自身的机制来生产所需的蛋白质。接下来,他们提纯蛋白质,这样他们就可以用两种方法中的任何一种来观察它的结构。一种是X射线晶体学,它涉及到生成纯蛋白质的微小晶体,并通过高能电子束的X射线轰击它们来揭示它们的内部结构;另一种是冷冻电子显微镜(cryo-EM),利用高倍电子显微镜扫描快速冷冻的蛋白质。
对于一种不熟悉的蛋白质来说,这两种过程都需要数月,甚至数年。幸运的是,许多新型冠状病毒蛋白都是“老熟人”,与SARS-CoV的序列相似性达到70-80%。SARS-CoV是导致2003年SARS爆发的病毒。早上7:30, Mesecar等人已经开始设计新的病毒蛋白质的基因结构,甚至预测现有的冠状病毒抑制剂可能会抑制这些蛋白质。
Satchell一直在关注有关这种病毒的早期新闻报道,他组织了一次由研究小组成员参加的虚拟会议,开始着手解决这种病毒的蛋白质问题。Satchell表示,他们把所有研究力量集中在COVID上。CSGID研究者Mesecar从Mpro着手。Mpro是病毒的主蛋白酶,一种从病毒侵入细胞时产生的长链上切下蛋白质的酶。没有Mpro,就没有病毒复制。人类没有类似的蛋白酶,所以针对这种蛋白质的药物不太可能引起副作用。
1月13日:42例确诊病例
在德克萨斯大学(University of Texas)奥斯汀分校McLellan的分子生物科学实验室,研究生Daniel Wrapp花了一个周末解析了另一种关键蛋白质的基因结构——冠状病毒的外部的、三个齿状的突起,这些刺突蛋白也就是冠状病毒名字的来源。1月13日,也就是星期一,Wrapp向一家商业公司下了订单。
McLellan曾参与确定另外两种冠状病毒的结构——HKU1和MERS病毒。HKU1是普通感冒的病因。这项研究是与加州拉霍亚市斯克里普斯研究所(Scripps Research Institute)的结构生物学家Andrew Ward和马里兰州贝塞斯达美国国家过敏和传染病研究所疫苗研究中心(US National Institute of Allergy and Infectious Diseases’ Vaccine Research Center)的病毒学家Barney Graham合作完成的。因此,研究小组知道如何调整这种刺突蛋白的基因序列,使其稳定在融合前的形状——它在进入宿主细胞之前所采用的形状。McLellan表示,他们获得这种特殊结构的能力来源于我们在研究HKU1、MERS和SARS时的所有先验知识。
当McLellan的团队在等待构建的基因片段到来的时候,Grapham给Moderna Therapeutics打了个电话。Moderna Therapeutics是一家位于马萨诸塞州剑桥的药物发现公司,疫苗研究中心(Vaccine Research Center)与该公司合作开展了一个预防大流行的项目。1月13日,在刺突蛋白未被合成之前,Moderna就开始准备其生产设备,以制造基于该蛋白的冠状病毒疫苗。
1月26日:2,014例确诊病例
在中国上海科技大学,饶子和与杨海涛等人夜以继日地工作,牺牲了他们为期一周的中国农历新年假期,来解决冠状病毒用来复制的Mpro结构和另外三种蛋白质的结构。
利用从上海同步加速器辐射设备(Shanghai Synchrotron Radiation Facility)和上海国家蛋白质科学中心(National Center for Protein Science Shanghai)获得的X射线数据,研究小组解决了Mpro与抑制物结合的晶体结构。2003年,他们花了两个月才解决了SARS-CoV Mpro的结构问题。这次,他们只花了一周。
冠状病毒中的Mpro由两个相同的亚基组成,看起来像被虫蛀的心脏,在结构的两侧各有一个活性酶位点。1月26日,杨海涛和饶子和将Mpro的结构数据提交给了蛋白质数据库(Protein Data Bank, PDB),这是一个用于存储生物分子三维结构的开放数字资源。2月5日,数据处理完毕,最终的结构已经在网上发布——杨表示,这一刻来得正是时候。该实验室已经收到了300多份关于这种结构的申请。
在研究Mpro的过程中,饶联系了他以前的同事、英国牛津大学(University of Oxford)的结构生物学家David Stuart。Stuart是英国同步加速器设备公司Diamond Light Source的生命科学总监。Diamond生命科学副总监Martin Walsh表示,来自英国和中国上海的团队开始密切合作,分享建议,避免重叠。他们让彼此了解最新情况,并试图从彼此使用的不同方法中获益。
由于上海的研究小组用一种抑制剂解决了Mpro复合物的问题,Diamond的研究小组决定专注于无分子连接的蛋白质结晶,希望找到潜在药物化合物可能结合的活性位点。Walsh的团队在两周里进行了1.7万个实验,试图找到将未结合蛋白质沉淀成晶体的最佳配方。
2月1日:确诊病例11,953例
在吕贝克大学(University of Lübeck)Hilgenfeld的实验室里,研究员张琳琳(Linlin Zhang)一直在打电话给这家每天研究Mpro基因构建物的公司,直到最终结构得到确定。由于实验室在结晶其它冠状病毒蛋白酶方面的经验,张在10天内培育出了Mpro晶体。2月1日,她将珍贵的样品带到柏林的BESSY II同步加速器,这为该项目开辟了一条专门的光束线。
除了专注于未结合的Mpro结构外,Hilgenfeld还将一种名为13a的小分子抑制剂加入到该蛋白的活性位点上。这种抑制剂是他设计用来抑制MERS病毒的。这并不是一个完美的组合,因此研究小组改变了化合物上的一种残留物,并将其命名为13b。Hilgenfeld指出,13b与Mpro的结合“非常完美”,他的团队在10多天后解析了Mpro与13b结合后的结构。
在德克萨斯州,McLellan的团队正在以同样的速度解决刺突蛋白质结构的问题。得益于价值数百万美元的低温电子显微镜设备,McLellan迅速收集了稳定脉冲的高分辨率电子显微镜数据,然后将数据发给了疫苗研究中心的Graham。
疫苗通常是基于将病毒的某些部分呈现给人类免疫系统以引起反应的,而刺突蛋白是一个明显的候选,因为它在感染中起着至关重要的作用。
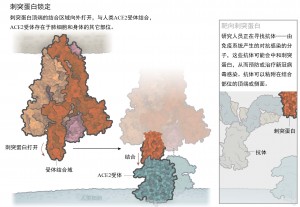
这个毛刺状的蛋白由三个相同的分子粘在一起形成一个金字塔的形状,它有一个铰链式的活动门结构。当“门”打开时,暴露的一部分蛋白抓住人体细胞上的受体(图“刺突蛋白锁定”)。Graham 和McLellan过去对一种类似的蛋白质所做的研究表明,将关闭状态的这种刺突蛋白呈递给免疫细胞,会刺激人类的免疫响应。从完整的结构中,Graham可以看到McLellan的基因构建产生了一个排列正确的高质量蛋白质。Graham表示,电子显微镜的信息是非常非常重要的。
Graham 在老鼠身上测试了这种刺突蛋白,试图改善其表达水平和对免疫系统的影响,并将序列发送到Moderna,那里的生产线已经准备就绪。2月7日,Moderna完成了基于该蛋白的第一批疫苗。
与此同时,在2月10日,也就是收获这种蛋白质的12天后,McLellan和他的团队向PDB提交了它的低温电子显微镜结构。通过对这种突变的详细研究,他们发现它与人类细胞受体(一种名为ACE2的蛋白质)的结合至少比SARS-CoV紧密10倍。
在圣保罗的明尼苏达大学(University of Minnesota),Li的团队正在研究原因。2月11日,Li等人开始使用先进光子源(Advanced Photon Source, APS),即位于伊利诺伊州芝加哥附近的美国能源部阿贡国家实验室(Argonne National Laboratory)的同步加速器设备,从刺突蛋白质中收集X射线数据。到2月13日,研究人员已经确定了一个小而重要的位点,在这个位点上,刺突蛋白锁定在ACE2受体上。他们发现与SARS-CoV相比,新型冠状病毒刺突蛋白的结合区域存在较小的分子差异,这可能是新型病毒与ACE2结合更强的原因。这些变化也可以解释为什么它似乎比SARS病毒更好地感染细胞和更快地传播。同一周,这种病毒也有了一个名字:SARS-CoV-2。
2月18日:73,332例确诊病例
到2月中旬,蛋白质结构数据大量涌现。2月18日,Hilgenfeld, Zhang等人单独提交了一篇关于Mpro结构并与13b结合的论文,并于2月20日在bioRxiv服务器上发布了预印本。Hilgenfeld承认,速度很快。最长的时间就是等待发表的时间。就在同一天,Diamond团队在其网站上发布了未结合 Mpro的高分辨率晶体结构。
为了支持美国团队,APS和其他国家同步加速器协调了它们的时间表,以确保在一个设施因维护或局部爆发而被迫关闭时,不会中断波束时间。APS的主管Stephen Streiffer表示,他们的目标就是让研究继续下去,科学家在处理这个问题上的速度比他们处理其它问题的速度快一个数量级。
到目前为止,CSGID联盟已经解决了12个独特的SARS-CoV-2蛋白结构,这些结构保存在一个新的在线数据库中,并附带了基因组信息。加州大学河滨分校(University of California, Riverside)的生物信息学家、性别认知障碍症研究者Adam Godzik指出,他们参与了类似的癌症研究项目,但花了5年才完成。但这次的研究是在几个月里自发发生的。
3月16日:167,515例确诊病例
有了3D结构,结构生物学团队直接进入下一步。Mesecar指出,结构不是一切,他们需要开发化合物——抗病毒药和疫苗。
3月16日,病毒基因组发布后仅仅65天,临床医生在美国国立卫生研究院(US National Institutes of Health)资助的一项临床试验中,给病人注射了Moderna的第一剂候选疫苗。
Graham表示,这比他们以前做的最快的还要快得多。由于对SARS和MERS的研究,冠状病毒可能是唯一能在这么短时间内被研究充分的病毒,如果是布尼亚病毒(bunyavirus)或沙状病毒(arenavirus),他们可能要花两到三年才能鉴定出结构。
但是,即使是以破纪录的速度开发的疫苗,也可能比重新利用已批准的药物或至少找到已开始进行安全测试的药物要慢。Satchell指出,这绝对是目前帮助住院病人的最快方法。
这正是Andrew Hopkins的计划。3月19日,位于英国牛津的人工智能药物研发公司Exscientia的首席执行官Hopkins送来了一个装着干冰的大型泡沫塑料冷却器。里面是加州斯克里普斯研究所(Scripps Research)寄来的一个包含1.2万种已知安全,且可供人类使用的药物化合物库。与Diamond密切合作的Exscientia团队立即开始针对Mpro、刺突蛋白、另一种蛋白酶和复制相关复合体进行药物筛选。Hopkins表示,Exscientia的科学家目前正准备测试结合前两种蛋白质的化合物的抗病毒活性。
与此类似,上海科技大学的团队对1万多种已获批准的药物和化合物进行了虚拟和高通量筛选,以确定是否有药物可以抑制Mpro。他们确定了6名有希望的候选药物。其中之一是ebselen。目前该药物处于临床试验阶段,研究人员正在测试其对双相情感障碍和听力损失的治疗效果。杨海涛表示,上海科技大学的团队正在准备动物实验,以研究其在体内的活动。
4月10日,杨海涛、饶子和等人发表了病毒复制复合体的结构——RNA依赖性的RNA聚合酶(RdRp,或nsp12)的大蛋白质,它与nsp7和nsp8组成复合体。他们还模拟了病毒与抗病毒药物瑞德西韦(remdesivir)的结合方式。瑞德西韦最初用于治疗埃博拉病毒,目前正处于冠状病毒的第三阶段试验。另一个最近完成的蛋白质与药物的复合物结构可以提供一个模板来帮助建模和修改其它现有的抗病毒药物。
4月22日:2,471,136例确诊病例
虽然设计全新的、自定义的药物来抑制SARS-CoV-2蛋白的核心生物化学需要几个月甚至几年,但最终可能研制出抗感染效果最好的药物。
上海科技大学的团队和合作者设计并合成了一系列针对Mpro活性位点的化合物。4月22日,经过大量化学修饰后,他们公布了一种抑制细胞内病毒复制的药物的细节,这种药物在大鼠和狗身上试验时无毒。杨指出,研究小组将继续开发这种化合物,以作为候选药物。
Diamond小组已经识别出91个与Mpro结合的化学碎片——小于正常药物三分之一大小的分子碎片。这些碎片激发了一个非盈利性的众包项目的启动——COVID Moonshot,邀请世界各地的化学家使用这些碎片来设计抗病毒药物候选。该计划已经收到了超过4,600份设计方案,一些治疗的可能性已经出现。
在德国,德国布赫姆霍尔兹感染研究中心(Helmholtz Centre for Infection Research)的研究人员Katharina Rox在老鼠身上测试了Hilgenfeld的13b化合物,结果显示它是安全的,在肺部这个关键感染部位积聚得很好。与此同时,Mesecar开发的一种抑制SARS-CoV的化合物在未发表的研究中被证明对细胞中的SARS-CoV-2具有抗病毒活性,他希望在今年夏天结束前完成动物研究。
5月14日:确诊病例4,248,389例
结构生物学家继续致力于研究冠状病毒基因组中剩余的未结合蛋白。其中包括ORF8,一种功能仍然很神秘的蛋白质。Godzik等人预测它应该是可以结晶的,但没有人做过,他们正在尝试。
在英国,Diamond团队正在筛选各种化合物以对抗第二种冠状病毒蛋白酶。在德克萨斯州,McLellan已经将刺突构造发送到全世界100多个实验室。许多人正在寻找治疗方法,用这种蛋白质从COVID-19患者的血液中提取抗体,McLellan的团队现在正在鉴定第一个可能具有治疗作用的抗体。
由于一项强制性的退休政策,Hilgenfeld原定于4月1日正式退休。他研究冠状病毒已经有20年了,但大多数时候它被忽视了,没有被认真对待。既然已经发生疫情,Hilgenfeld怎么能在这个时候离开呢?他的团队正在研究其它SARS-CoV-2的结构,包括nsp3,一种病毒用来关闭宿主细胞防御的大型蛋白质。
对抗病毒的竞赛不能在短时间内放慢速度。Satchell指出,一旦各国开始解除对人员流动的限制,病毒就会卷土重来,再次席卷全球。当这种情况发生时,能有专门针对这种冠状病毒设计的漂亮药物就太好了。但我们需要尽快行动。
原文检索:
Megan Scudellari. (2020) The sprint to solve coronavirus protein structures — and disarm them with drugs. Nature, 581: 252-255.
张洁/编译