医疗科技新进展
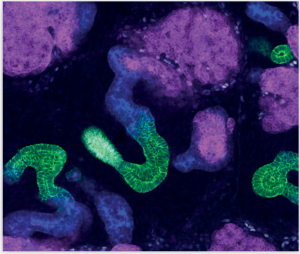
类器官(Organoids)能模拟各大器官和组织的早期发育过程。
医学技术和设备的快速进步,让我们有机会开发出新的治疗手段和药物。
1. 类器官
所谓类器官(Organoids),指的就是用于实验测试的小型器官模型。
十年前还没有类器官(Organoids)这个词。今天,它已成为生物医学领域里最火的词儿,可用于形容三维多细胞结构(three-dimensional multicellular structure),或者迷你器官(mini organ)。得益于多潜能干细胞(pluripotent stem cell, PSC)技术的进步,我们有机会通过类器官来加深对体内各器官的功能和疾病的认识,有机会开发出新型的药物筛选平台和个性化医疗项目,减少我们对动物实验的依赖。
人体内的任何细胞,比如皮肤细胞或白细胞等细胞,都能够培育成PSC。这些PSC具有同胚胎细胞(embryonic cell)一样的分化特点,但是却没有胚胎干细胞需要面对的伦理问题,因此,利用PSC可以培育出任何人体细胞。这些细胞在实验室里还能够自我组织在一起,形成具有三维立体结构的、能模拟各大器官和组织的早期发育过程的类器官。
2015年,《自然》(Nature)曾发表过一篇重量级文章,介绍了澳大利亚墨尔本的默多克儿童研究中心(Murdoch Children’s Research Institute in Melbourne, Australia)干细胞生物学家Melissa Little等人开展的一项开创性的工作。科研人员利用PSC培育出了人体肾脏里的20多种不同的细胞,而且还让这些细胞自我组织,形成了一个复杂的器官模型。这项工作表明,我们有能力在实验室里创造出一个复杂的组织,让细胞自我交流,并形成复杂的结构。
自此之后,又有很多科研人员开发出了更多的、以PSC为“原材料”的各种类器官,以及培育复杂组织的试验方法,比如食道(oesophagus)、肺、胃、结肠、胰腺、肝脏、小肠、甲状腺、眼和脑等多种类器官。
虽然类器官是帮助我们了解组织发育的极好模型,但是Little还希望做到尽善尽美,于是他又和生物工程学家合作,让这些类器官在培养皿里继续生长,用于后续的研究工作。2018年,Little等人将一个人体类器官移植到了小鼠体内,结果小鼠的血管长入了这个外来的移植物里,人体类器官在小鼠体内继续生长、并发育成熟。
在过去使用动物模型从事药物开发时,有很多药物在动物实验里的结果都很好,可是到了人体实验阶段就失败了。Little表示,如果我们能够在实验室里培育出更成熟的组织和类器官,来取代动物模型,就有可能解决这个问题。
2. CRISPR技术
分子神探。
1987年,科研人员在大肠杆菌的基因组里发现了一段不寻常、且功能不明的重复DNA片段。三十年之后,这个DNA片段成就了生物医学史上最重大的一项发现。
这就是CRISPR序列,它与Cas9酶一起,原本是细菌抵御病毒感染的武器,却成为了科研人员手中,有史以来最完美的DNA编辑工具。
目前,这套CRISPR–Cas9系统已经用于在动物模型中治疗癌症和HIV病毒感染,也用于开发抗旱转基因农作物,以及消灭蚊虫等科研工作。去年,这项技术也成为了全世界聚焦的中心,引起了巨大的争议,因为中国的科研人员贺建奎在2018年底时宣称,他们利用CRISPR–Cas9技术对胎儿进行了基因改造,并诞生了世界上第一例基因编辑婴儿。
虽然CRISPR–Cas9技术成本低廉,功能强大且高效,但也并非十全十美。比如该技术会导致大规模的、不可预测的脱靶遗传修饰(off-site genetic modification)。目前,科研人员正在积极地开发各种人工修饰Cas9蛋白,来解决这个问题,降低差错率。
同时,科研人员也在开发侵入性更低的CRISPR应用技术,还在探索CRISPR技术的诊断潜力,比如对尿液、血液和唾液进行检测,了解是否感染了埃博拉病毒(Ebola virus)、寨卡病毒(Zika virus),以及是否患上了肺癌等。
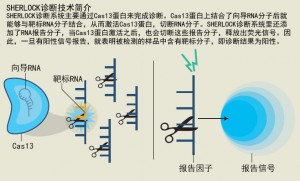
SHERLOCK就是这样一种诊断工具,这是一种类似于早孕试纸一样的试纸条样的诊断工具,可以对血样进行检测,了解是否存在特定的分子目标。SHERLOCK中使用的是Cas12a(又名Cpf1蛋白)和Cas13蛋白。这套系统可以同时检测多达四种目标,主要作用机制就是根据检测目标,人工合成相应的RNA片段,然后利用Cas蛋白对其进行切割,完成检测(图“SHERLOCK诊断技术简介”)。
SHERLOCK系统是由美国博大研究院(Broad Institute of MIT)和哈佛大学(Harvard in Cambridge, Massachusetts)联合开发的,价格非常便宜,完成一次检测仅需要花费0.61美元,而且可拓展性非常高,能够针对各种靶标完成检测。生物医学工程师Omar Abudayyeh表示,SHERLOCK系统在很多领域都具有非常激动人心的应用潜力,比如可用于检测细菌、病毒、肿瘤,也可用于现场检测(point-of-care detection)、基因分型(genotyping),以及农业等领域。
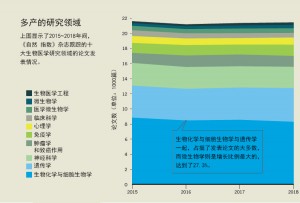
目前有越来越多类似SHERLOCK系统的CRISPR应用,都在使用Cas9蛋白之外的其它Cas蛋白。这些Cas蛋白的种类也越来越多。2015年,《细胞》(Cell)杂志就首次发文介绍了Cpf1蛋白的应用潜力。据跟踪各杂志顶级生物医学论文的《自然 指数》(Nature Index)的统计,该文章的引用率目前排在第30位。
3. 新型抗生素(ANTIBIOTICS)
寻找新型抗生素的工作催生出一系列非常有前景的细菌发掘新方法。
上世纪40年代至60年代初是抗生素开发的黄金时代,当时,几乎所有能够在培养皿里生长的土壤微生物和海洋沉积物(marine sediment)微生物都被科研人员研究了个遍,找到了各种各样的抗生素。可是几十年过去了,病原体也已经对这些抗生素产生了耐药性(resistance)。而后来出现的人工合成抗生素也没能解决耐药性的问题。
在全球寻找新型抗生素的竞赛里,出现了几种极富潜力的新型抗生素开发技术。
其中之一就是美国东北大学(Northeastern University in Boston, Massachusetts)的生物学家Slava Epstein和Kim Lewis在2009年合作开发的iChip平台。该技术能够分离单个细菌,然后在原位土壤中继续培养(培养板底部有一层半透膜,下面土壤里的营养物质可以透过这层半透膜,供养细菌),形成菌落。这种细菌培养板为其它99%的“微生物暗物质(microbial dark matter)”,即以前尚未被发现的天然抗生素提供了出口(doorway)。利用以往的细菌培养方法,是很难发现这些天然抗菌物质的。
Epstein和Lewis在美国马萨诸塞州坎布里奇市联合成立了NovoBiotic制药公司(NovoBiotic Pharmaceuticals in Cambridge, Massachusetts),继续开展他们的新型抗生素研发工作。他们已经发现了teixobactin,这种新型抗生素能够与细胞壁里的两种组份结合。因此,细菌很难对其产生耐药性。他们的工作于2015年发表在了《自然》(Nature)上。据《自然 指数》的统计,该文章也位列近3年来十大最具影响力文章的行列之中。
NovoBiotic制药公司的科研人员Amy Spoering还发现了另外一种新型抗生素,该物质的作用机制与teixobactin类似。他们也发现了许多其它的新物质。
Lewis等人计划在今年晚些时候公布他们在iChip平台上取得的最新研究成果——第三款新型抗生素。这种抗生素能够杀死包括大肠杆菌(E. coli)、绿脓杆菌(Pseudomonas aeruginosa)和肺炎克雷白杆菌(Klebsiella pneumoniae)等难治性细菌在内的多种病原体。这也是目前临床上亟待解决的问题,因为其中有很多细菌已经对目前已知的所有抗生素全都产生了耐药性。
Lewis表示,正是因为这些科研成果,才让他比2015年时更加有信心去解决细菌对抗生素的耐药问题。不过未来的路还很长,因为目前的研发进展还是太慢了。
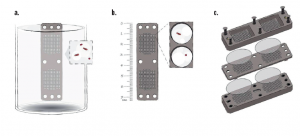
ICHIP平台简介:
a. 将一块含有大量小孔的培养板浸入含有大量微生物的液体里。
b. 稀释菌液,使每一个小孔刚好含有一个细菌菌体。
c. 在培养板的两面都盖上半透膜,然后加压固定,这样就形成了一个个微小的细菌培养皿。
4. 细胞疗法
按下肿瘤细胞的重启键。
CAR T细胞疗法(CAR T-cell therapy)能够激活人体的免疫系统去消灭癌细胞,但是昂贵的治疗费用限制了它的应用和推广。经过人工遗传改造之后,这种技术有望惠及广大肿瘤患者。
现代制药工业已经被两大类药物完全占据,那就是市场上最多见的化学合成的小分子药物(chemically synthesized small-molecule drug)和价格更高一点的生物大分子类药物,如蛋白质类药物。细胞类药物(Cellular therapy)则是新近出现的第三类药物,其中包括新型的疫苗、心肌再生药物和抗癌药物。
这些细胞类药物与传统药物完全不同,它主要利用活细胞来进行疾病的治疗。比如目前开发的最成熟的CAR T细胞类药物,就是肿瘤患者的新希望,它能够极大地改善传统抗癌疗法失败患者的病情。
CAR T细胞能够使人体免疫系统重启,治疗白血病(leukaemia)和淋巴瘤(lymphoma)等血液系统肿瘤的效果非常好。我们先提取患者自身的T细胞,然后对其进行人工遗传学改造,“装配上”人工合成的嵌合抗原受体(synthetic chimaeric antigen receptors, CAR),这些人工嵌合抗原受体能够与肿瘤细胞上的某些蛋白质结合。然后再将这些改造好的CAR T细胞注射回患者体内,就能够发挥靶向性的抗癌功效。
虽然在急性B淋巴细胞性白血病(B-cell acute lymphoblastic leukaemia)临床试验中发现,CAR T细胞的反应率(response rates)超过了90%,但有很多患者治疗后又出现复发的情况,而且治疗的副作用也非常大。目前,FDA只批准了Kymriah和Yescarta这两种药物上市销售,它们一次治疗的费用分别就高达47.5万美元和37.3万美元。
如此高昂的药价本身就反映出一定的问题,即我们目前很难持续地、成规模地生产活细胞类药物,因为谁也无法预测细胞培养环境会对这些脆弱的、各式各样的活细胞产生何种影响。
另外一大难题就是CAR T细胞对肺癌、乳腺癌和前列腺癌等实体瘤的治疗效果还很差。与血液系统肿瘤相比,这些实体瘤的遗传异质性更加复杂,更难找到合适的肿瘤特异性抗原靶标。
不过,2017年,美国纽约斯隆凯特林研究所(Sloan Kettering Institute in New York City)的科研人员在《自然 研究》(Nature study)杂志上发表了一篇文章,介绍了他们使用CRISPR–Cas9技术打造CAR T细胞的工作,这项技术创新有望极大地降低CAR T细胞的制备成本。
据斯隆凯特林研究所的免疫学家Michel Sadelain介绍,如果我们可以从遗传学的角度,对T细胞进行更好的改造,那么就可以用更少的CAR T细胞来开展治疗。
除了改造T细胞之外,肿瘤研究人员也正在开发“超级抗癌细胞疫苗(super-vaccines)”,不过这项工作目前还处在研发的初期阶段。
树突状细胞(dendritic cell)能够处理掉可能对人体有害的物质,并且“通知”T细胞来消灭这些有害物。因此,从理论上来看,这种疫苗可以解决肿瘤细胞的免疫逃避问题(即肿瘤细胞抑制人体天然免疫反应的问题)。
我们还可以用细胞类药物来治疗心脏病。比如,可以使用人体PSC开发出心肌再生药物,逆转心肌组织的损伤,诱发保护性反应。不过与其它细胞类治疗一样,这种疗法也极富挑战性,但治疗前景也是非常诱人的。
原文检索:
JENNIFER COOKE. (2019) TECHNOLOGIES TO TREATMENTS, NATURE INDEX: S10-S12.
Eason/编译