更大规模、对象更多样的基因测序研究
基于DNA的精准医疗需要更多的多样性来避免有害的偏见。一个大的研究项目的目的就是能解决这个问题。
大约20年前,当第一个人类基因组测序竞赛结束时,我为即将发生的事情激动不已。这是一个新世纪的黎明,而我们似乎正处在揭开生命蓝图——DNA背后的意义——的风口浪尖。一旦我们能排列出人类基因组中所有31亿个碱基对的分子,我想——那时我还是一名本科生,被科学学科弄得晕头晕脑——我们就能理解关于人类健康和疾病的一切。
我不知道的是,最初几十年的基因医学会把很多人忽略了。因此,几年后,也就是2009年,我刚拿到分子遗传学博士学位时,就被有关数据吓了一跳。当时,杜克大学(Duke University)的研究人员报告称,我们收集的基因组数据中,96%来自欧洲血统的人。这并不是少数人得出的结果:他们基于当时分析的170多万个个体基因组样本计算出了百分比,发现这些样本缺乏人口多样性。在接下来的几年里,情况并没有好转,就在4年前,基因组数据库仍然处于失衡状态,欧洲人的代表性增加了,其他所有人种的代表性减少了。
这种不平等如果得不到解决,就会变成巨大的健康不平等。现在,越来越多的人得到关于他们疾病的潜在原因的答案,因为医学能够挖掘他们的基因组。有数百种药物的标签含有遗传信息。鉴于基因变异会影响身体处理这些药物的方式,所以了解病人携带的突变有助于医生为病人设定最有益的剂量。此外,现在对不同癌症的基因组驱动因素的认识的提高,在医生诊断和治疗许多肿瘤方面带来了好处。然而,非白人和非男性的人有不同的基因,并不总是适合这些治疗方案。
例如,非裔美国人和拉丁美洲人的哮喘发病率在美国最高,但研究表明,吸入器中使用的普通药物对他们的有效率远低于对白人的有效率。服用抗冷冻药物卡马西平的亚洲人发生严重反应的风险更高,有时甚至致命。在开发这些药物时,没人会预料到这些问题。如果DNA是我们寻求更有效医疗的一个重要因素,那么我们就需要解决基因数据缺乏多样性的问题。
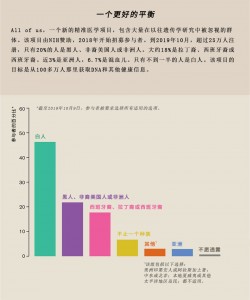
这是我们All of US的研究计划希望能解决的问题。All of US由NIH成立,并于2018年启动。该计划邀请了100万或更多来自不同遗传背景的人成为研究的合作伙伴,而不是人类受试者对象,并请他们分享一生的各种健康信息。我们已经有超过250,000名参与者。超过51%的人属于少数人种和少数民族,超过10%的人属于性别少数民族,总的来说,超过80%的人代表了一个历史上在研究数据集中代表性不足的群体。
人们可以通过访问这个计划的网站(www.joinallofus.org)并单击“立即加入”来加入我们。在同意参与后,受访者可以向我们提供他们的医疗记录,回应关于他们健康和生活方式的各种调查,并参与其他活动,如将他们的健身跟踪数据同步到我们的数据库中。我们在全国各地的地方医院和健康中心也有数百个登记点,参与者可以在那里提供血液和尿液样本,帮助研究人员研究他们的DNA。我们希望人们能坚持10年或更长时间,因为随着项目的发展,我们会定期为他们增加新的方式来了解自己,并为研究做出贡献。
是时候做出改变了
许多参与者-研究者合作都与技术进步有关。第一个人类基因组的测序费用达到10亿美元。如今,个体基因测序成本不到1000美元,而且可以在24小时内完成。将这些信息与其他重要的医疗数据结合起来也更容易。医疗机构已经把病人的纸质病历变成了电子版。截至2017年,96%的美国医院和80%的办公室医生正在使用经认证的电子健康记录系统。智能手机和智能手表等其他数字健康技术上的新应用程序可以直接从人身上收集数据。这些趋势都使得存储、共享和挖掘大型数据集以回答有关疾病原因和影响的问题变得更加容易。这种趋势还引发了隐私方面的担忧,这使得在项目中保证个人数据的安全性和透明性变得尤为重要。
把参与者当作伙伴是至关重要的。过去医学研究人员的行为在少数民族社区引发了很大的信任危机,因为他们在塔斯基吉梅毒研究(Tuskegee Syphilis Study)中给少数民族社区造成了极大的伤害,研究人员以400名非洲裔黑人男子为试验品秘密研究梅毒对人体的危害,不给予他们足够的治疗。此外,被广泛使用的HeLa细胞,来自一位名为Henrietta Lacks的病人,但研究者并未获得Lacks本人的知情同意。人们都希望看到研究向前发展,但是他们希望是作为合作者来参与项目,而不是受试者。为了克服这种不信任,我们所有人都在使用一种新的研究模式,即邀请参与者以及拥有科学学位的研究人员加入。参与者在项目的咨询和管理机构、工作组和工作组中任职。我们还与当地的医疗机构、医院和社区团体合作,为我们提供建议,帮助人们参与其中。社区参与对于大型医学研究项目来说并不熟悉,我们仍在学习最佳的方法。
一些已经让医学变得更好的研究为我们提供了发展长期关系的蓝图。例如,弗雷明翰心脏研究(Framingham Heart Study)始于1948年,受试者来自马萨诸塞州一个城镇的5,209名男性和女性,大部分是白人。这个研究有99%的保留率,一直持续到今天。当参与者年复一年地分享数据时,研究人员可以看到他们的心脏健康如何随着时间的推移而改变。弗雷明翰研究所确定的心脏病危险因素,如高血压、高胆固醇、吸烟和肥胖,在医疗方法中根深蒂固,甚至形成了常识。
更进一步
这种医学发现正是All of Us所设想的。但我们想更进一步,我们希望参与者不仅包括白人,还要具有更大的多样性,不仅仅是种族上的多样性,还要有很多不同的背景(如经济背景和地理背景等)。如果我们要找出健康和疾病的根源,这就意味着要了解我们所有人之间的差异和相似之处。例如,当个体携带了两个拷贝的血红蛋白基因突变时,镰状细胞病就会发生。镰状细胞病影响了10万名非裔美国人和全世界2,000多万人。相比之下,镰状细胞特性——个体只携带一个拷贝的突变基因——会赋予个体在打败疟疾上的优势,如果你的祖先来自疟疾流行的非洲等地区,这在进化上是有意义的。然而,新的研究发现镰状细胞特性可能不像医生过去认为的那样良性,因为它可能增加患肾病的风险。一些非裔美国人更容易受到这种风险的影响,有些则不那么容易。很明显,我们还缺乏很多信息来了解为什么会出现这种情况,以及不同的DNA变异如何相互作用,从而影响镰状细胞特征患者的健康。来自100多万名参与者的DNA信息可以帮助研究人员更多地了解像这样的复杂特征。
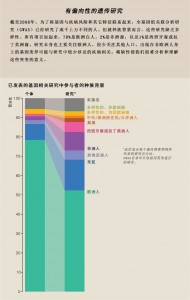
我们必须从一些广泛的分类开始,招募足够的参与者,然后再进一步细分组别。目前,我们已经超前完成目标,即更多地代表在研究中历来代表不足的群体。例如,非裔美国人约占美国人口的13%,但仅占先前用于基因组研究的样本的3%。到目前为止,在All of Us项目中,21.5%的参与者是非裔美国人。同样,拉美裔约占美国人口的18%,但在2016年,在基因组数据库中,拉美裔只占不到1%。而在我们的研究中,17.6%的参与者是西班牙裔。
这种多样性将帮助我们发现更多关于DNA如何影响不同社区的健康的信息,但DNA并不是我们唯一的关注点。当涉及到疾病时,基因之外的许多因素都在起作用。我们知道你出生在哪里、你吃什么、你感觉到的压力,以及其它临床和生物学因素都会影响健康,但我们仍然不知道它们各自对健康的影响有多大。例如,当我们想到影响我们人口的一些最常见的慢性病(如高血压)时,许多慢性病不成比例地影响到美国最弱势的社会和经济群体。从目前的情况来看,决定因素不仅仅是他们的种族或种族。风险还包括家庭结构、社会经济状况、创伤等压力源、性别和性别不平等、营养情况、获得医疗保健的机会,以及我们可以从All of Us的数据集中捕捉到的许多其它因素。
接下来的几年,我们应该能够将这些丰富的信息与参与者的DNA进行比较。当我们这样做的时候,所有人都将开始更清楚地了解生物学和环境在疾病发展中所起的作用,以及最重要的,我们能做什么。
原文检索:
Stephanie Devaney. (2019) All of us. Nature, 576: S15-S17.
张洁/编译