人类3D干细胞
微流体装置,例如这种“芯片肺”可用作干细胞生物学家的精细的研究工具。
人类干细胞产生的3D微型组织,可用于在体外研究正常人类生物学和人类疾病。
日本庆应大学医学院(Keio University School of Medicine)的干细胞研究人员Toshiro Sato在实验室的显微镜下观察了一个培养皿。不过他看到的不是一片细胞,而是更复杂的结构——肉眼几乎无法看清的球形组织。这些组织就是类器官。在适当的环境条件,干细胞会分化,并排列成与特定组织或器官类似的3D结构。
类器官可由多潜能干细胞(具有分化成任意身体组织类型,例如肌肉、皮肤、肠道和大脑的潜能)分化形成。当在合适的条件下生长时,例如使用特定的生长因子时,干细胞自我组织成与体内组织类似的、由不同细胞组成的结构。相比之下,芯片器官(organs-on-chip, OOC)通常通过将干细胞和已经分化成所需细胞类型的细胞按照位置和结构布置在微型装置上。英国剑桥医学研究委员会分子生物学实验室(MRC Laboratory of Molecular Biology)的发育生物学家Madeline Lancaster指出,类器官与OOC之间的区别在于“是自组织,还是人工构建”。
类器官被评为了去年《自然》(Nature)杂志的年度技术,并越来越多地被用于研究正常发育和疾病进展。例如,Sato的研究小组利用类器官来研究肿瘤形成的早期阶段。他的研究小组使用CRISPR基因编辑技术来改变干细胞中的DNA序列,然后研究这些突变如何影响类器官的发育。Sato表示,这种方法通过测试特定突变是否会重演癌症发展来研究因果性。
类器官和OOC在评估药物、化学品和化妆品的功效和安全性方面也很有潜力,并可能被应用于再生医学。哈佛大学(Harvard University)怀斯生物启发工程研究所(Wyss Institute for Biologically Inspired Engineering)的创立者Donald Ingber举了个例子:随机临床试验面临的挑战是如何比较治疗效果,因为参与者的遗传学和生活史可以影响他们对候选药物的反应。来自患者细胞的OOC和类器官具有相同的遗传学和临床历史,因此可以消除这些混杂效应。然而,这些技术还有待进一步发展,例如如何扩大生产规模以满足不断增长的基础和应用研究需求,同时提高可重复性,并保持类器官和OOC与其所代表的体内器官的保真度。
培养皿里的器官
研究人员用来制造类器官和OOC的多潜能干细胞包括天然胚胎干细胞(embryonic stem, ES),以及通过诱导已分化细胞(如成纤维细胞)而得到的、具有多能性的细胞,即诱导多潜能干细胞(induced pluripotent stem cell, iPS细胞)。Lancaster利用类器官来研究基本的大脑发育,并确定自闭症和精神分裂症等复杂疾病的诱发因素,同时使用ES细胞来开发和测试研究方案和新模型。
用于研究遗传性疾病或个性化药物的类器官通常由成体干细胞或iPS细胞制成,这些细胞经过改造后具有患者特异性。荷兰乌得勒支干细胞与发育生物学研究所(Hubrecht Institute)的遗传学家Hans Clevers利用源自肠干细胞的类器官来预测囊性纤维化患者对各种药物的反应。囊性纤维化可由单个基因CFTR中的任何突变引起。尽管临床上已有囊性纤维化的疗法,但是非常昂贵,且仅适用于具有特定突变的患者。Clevers的研究小组现在正在测试源自荷兰600名不携带这些突变的囊性纤维化患者的类器官。其基本原理是,如果药物能导致患者的类器官在测定条件下膨胀,那么患者也可能对该疗法产生反应。
同样,Sato的团队也开发了一种使用成体干细胞产生肠类器官的方法。他现在正参与一项临床试验,以测试由8名患者的干细胞制成的组织是否可被安全地植入肠道,以修复由溃疡性结肠炎引起的损伤。
在癌症研究和药物开发中,类器官已经证明了自身的价值。国际人类癌症模型计划(International Human Cancer Models Initiative)正在开发“二代”类器官模型,其中某些DNA序列已被注释。通过研究临床数据,研究人员可以将他们在类器官上的发现与患者特征和结果联系起来。美国国家癌症研究所癌症基因组办公室(National Cancer Institute’s Office of Cancer Genomics)的主任Daniela S. Gerhard表示,今年晚些时候,人们就可以从美国典型培养物保藏中心(American Type Culture Collection, ATCC)订购这些类器官了。ATCC最开始将提供约150种不同的类器官模型,目前售价尚未确定。由Clevers担任首席科学家的Hubrecht类器官生物样本库(Hubrecht Organoid Technology biobank)提供了数百种来自成体干细胞的不同类型的器官,价格在2000到3000欧元之间(折合1700-2600美元)。Clevers等人使用来自18名患者的结肠直肠癌细胞衍生的类器官来检测83种抗癌化合物。类器官中的耐药模式与已知的耐药突变相对应,表明类器官可用于预测患者对特定药物的反应。
Clevers指出,由ES细胞和iPS细胞衍生出来的组织是研究复杂的发育过程的理想模型,但它们的生产周期较长,可能需要数周或数月;若由成体干细胞构建类器官,则生产周期短一些。由于构建时间短,被引入突变的概率也更小,因此相对于ES和iPS,由成体干细胞构建的类器官的重现性更好。
培养类器官的过程类似于标准的组织培养工作。Sato表示,即便是新入门的研究生,也可以在几周内轻松培育出类器官。Lancaster补充,由干细胞构建组织是一件很容易的事,难点在于结果解读。我们很难确定得到的类器官更像哪些真实组织。
OOC的一致性
有时也被称为微生理系统或组织芯片的OOC是一种可用于培养细胞的、名为微流控芯片的结构化微型器件。与干细胞自发发育的类器官不同,OOC的发育过程是被设计好的。芯片的结构以及细胞的类型和位置决定了出现的组织及其排列方式。对此,加拿大麦克马斯特大学(McMaster University)的生物工程师Boyang Zhang表示,这意味着OOC通常比类器官更稳定。当然,OOC也可能更复杂,因为开发人员可以添加工程元素,如传感器、促进流体和气体交换的“脉管系统”,以及便于成像的元素,这些元素不能自发地出现在类器官中。
我们可以购买某些组织芯片。开发OOC的生物工程师可以从企业或科研机构那里获得他们的初始芯片。Wyss研究所的一个研究小组利用涂有合成聚合物的显微镜载玻片制成了“芯片心脏”。采用患有先天性心脏病的Barth综合征患者的iPS细胞,研究小组首先诱导iPS细胞分化成心肌细胞,然后在芯片上培养这些细胞以产生可测试功能的组织。研究人员能够证明与Barth综合征相关的突变导致心肌细胞功能异常。他们也能够在体外纠正缺陷。
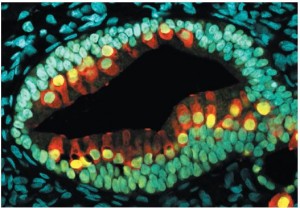
内耳类器官的横截面。
由Zhang共同创立的TARA Biosystems公司开发了一种名为Biowire的心脏OOC,以用于药物测试。TARA科学家将来自iPS细胞的心肌细胞放入一个微型装置中,细胞会围绕装置中的一根细丝生长。这有助于引导心肌细胞按照功能所需的常规结构进行排列。发育中的“心肌”在电刺激诱导下,成为可以收缩和放松的成熟心肌,并且可以模仿真实心脏组织的功能。例如,施加肾上腺素,心脏OOC收缩会增加。
Nortis公司通过玻璃纤维周围的固化胶原基质来创建OOC,然后将玻璃纤维去除,得到数毫米长的、直径约100微米的空心通道。一旦往管道里接种细胞,组织就会在几天内形成。这种芯片是一次性的,可以运行三个并行实验,售价300美元。
Nortis首席执行官Thomas Neumann表示,干细胞生产OOC的优势将更加突出,因为干细胞在再生医学和个性化医疗上具有重要潜力。但是,他也指出,如果干细胞产生的OOC没有完全分化或成熟,就会产生问题,所以质量保证将变得更加重要。
OOC可被设计成具有很高的复杂度,而这是类器官无法比拟的。例如,OOC可以用来模拟生理特性,如组织拉伸、脉动和蠕动。Ingber在2010年发表的关于肺毛细血管—肺泡界面的微型模型的论文创造了“芯片肺”,开辟了这一领域的先河。芯片上的通道由一侧分隔肺泡细胞,另一侧分布血管细胞的膜分开。而呼吸则可以通过向侧室抽吸空气来模拟。Ingber指出,机械微环境对于获得体内功能至关重要。该团队使用这种模拟呼吸系统来测试纳米粒子的毒性。
我们也可以将多个OOC连接在一起,创建多器官的“芯片身体”模型。康奈尔大学(Cornell University)的生物工程师Michael Shuler的团队已经制作出了一个封闭的OOC系统。该系统有14个腔室,代表具有“屏障”功能的器官,例如肺部中的肺泡,以及“非屏障”功能的器官,如心脏中的组织。
麻省理工学院(Massachusetts Institute of Technology)的生物工程师Linda Griffith等人成功建立了一个十器官系统,其中物质可以从一个器官流到另一个器官,就像它在身体中的输送一样。一些器官,如“大脑”,起源于iPS细胞;而包括“肝脏”在内的其它器官则来自细胞系或其它分化细胞。该组织可以存活四周,并且该系统具有一定的生物学功能。例如,从肠道组织进入系统的药物被传递到肝脏,在肝脏被代谢。Griffith表示,该项目费时、费力还费钱,而且涉及多学科协作,不仅需要生物工程师和机械工程师,还需要建模者将芯片的数据解读成相应的人体过程。实际上,科学家通常只用连接2到4个OOC就非常合适了。
OOC的开发者现在正在着眼于向行业和监管机构展示该技术的价值和有效性。扩大OOC的使用将需要更易于批量化生产的构建方法和高通量应用。多个OOC连接的系统面临的一个挑战是寻找适合所有组织类型的培养基和培养条件——例如,支持肝细胞的培养基并不一定适用于肺细胞。实现准确的模型还需要调整细胞数量和各种芯片的活动,以便准确地模拟这些器官在人体中的功能。Ingber认为,总的来说,OOC领域将变得更具用户友好性。它已经到了即插即用的地步,你不需要成为微系统工程师就能使用OOC。
展望未来
随着类器官和OOC使用的日益广泛,研究人员下一步便是着手解决更复杂的问题。Griffith等人正在将肠道微生物群添加到他们的系统上,如已连接肠道、肝脏和大脑以研究帕金森病的模型。她指出,随着成本的下降和可重复性的提高,OOC可能会开始替代实验动物,从而成为人类受试者的替代物。若从工程化的角度出发,那么在生物学上我们目前仍处初期阶段。我们该思考如何用这些简约模型来正确地表征生物系统。
Ingber的研究小组以类似芯片肺的方式使用OOC,以创建肺部气道片来测试香烟烟雾带来的影响。该模型允许研究人员分析在吸烟和不吸烟两种情况下,来自相同人类供体的组织的基因表达谱的差别。
虽然类器官和OOC各有其拥护者,但其实二者可以从根本上回答相同的问题。它们之间的界限已经模糊。Zhang希望在接下来的几年里,能看到将二者结合,各取所长的论文。Zhang倡导所谓的协同工程:基于自组织和发育的相关知识,开发OOC上的类器官。他设想将OOC的受控结构、内置读出和机械能力与类器官对组织和器官特征的保真度结合起来。Lancaster和其他人正在积极努力,将类器官和OOC研究人员聚集在一起——例如,举办研讨会分享难点、方法和想法。她指出,对于科学而言,合作比各自为战有效得多。跨领域合作,才能收获最多。
更多阅读:芯片模型
类器官和芯片器官(OOC)可用于药物开发、化妆品检测、毒理学和个性化医疗。以下是它们的一些优点和缺点。
类器官
来源:由自组织ES细胞、iPS细胞或成体干细胞产生。
主要优势:可用于研究单细胞发育成器官的过程,以及发育疾病中的相关过程。
未来发展:提高需要获得稳定测试结果,如药物测试的可重复性和实用性;并找到构建类器官中的血管的方法。
了解更多信息:Cell Press webinar ‘Organoids and beyond — 3D tissue in a dish’ (see go.nature.com/2jiumvb)
OOC
组织来源:通常来自从人体分离的细胞系或分化细胞,但也可以来源于干细胞。
主要优势:重复性和一致性,可加入生物力学特征。
未来发展:使用iPS细胞和干细胞,而非来自患者的细胞系来构建,以增加对个性化药物的适用性。
了解更多信息:National Academies of Sciences, Engineering, and Medicine webinar ‘The NIH Microphysiological Systems Program’ (see go.nature.com/2hm3bch)
原文检索:C. Y. Tachibana. (2018)Stem-cell culture moves to the third dimension. Nature, 558: 329-331.
张洁/编译