肾癌新发现,ZHX2是VHL靶点
透明细胞肾细胞癌(Clear cell renal cell carcinoma, ccRCC)是肾癌的一种亚型,它其中一个特征是约90%的ccRCC患者的von Hippel-Lindau(VHL)基因失活。VHL是E3泛素连接酶复合物(通过靶向脯氨酰-羟基化的蛋白质,来发挥蛋白酶体降解的作用)的底物识别亚基。VHL的典型靶标是缺氧诱导因子(hypoxia-inducible factor, HIF,一种在富氧条件下不稳定的转录因子)的α亚基。HIFα在ccRCC发育早期成为稳定因子,诱导促进血管生成和细胞内代谢重编程的转录活动的发生。寻找HIFα以外的、逃脱被降解命运,并促肿瘤发生的VHL底物是一种潜在的ccRCC新疗法。最近一期的《科学》(Science)杂志上,Zhang等人发现了一种新的VHL靶标ZHX2(zinc fingers and homeoboxes 2)。ZHX2通过调节核因子B(NF-KB)信号传导来促进ccRCC肿瘤发生,它可能是治疗ccRCC的新靶标。
ZHX DNA结合蛋白家族通过其作为转录抑制因子的功能在细胞周期进程中发挥关键作用,抑制细胞周期蛋白依赖性激酶的表达。转录组的分析显示,与健康肾组织相比,ccRCC患者肾脏中ZHX1和ZHX3基因表达减少,而ZHX2基因在肿瘤中过表达。ZHX1和ZHX3在ccRCC肿瘤中的低表达也与较差的总体患者存活率相关,这与它们作为细胞周期进展抑制剂的确定作用一致。然而,科学家对ZHX2在ccRCC中的功能及其作用机制知之甚少。此外,ZHX2作为细胞分裂负调节因子的潜在作用令ZHX2在肾癌中的过表达现象显得有些异常。
Zhang等人使用一种体外筛选的方式来鉴定ZHX2。使用原发ccRCC患者的组织样本,他们发现,ZHX2在缺失VHL的细胞核中积累,而无VHL缺失的ccRCC组织中则不存在这种现象。ZHX2在细胞模型以及小鼠模型上,都具有维持多种ccRCC细胞系的增殖的功能。
为了确定ZHX2在ccRCC中的促癌机制,Zhang等人使用全基因组方法,发现ZHX2能正向调节许多NF-KB靶基因的表达。在VHL基因失活的ccRCC中,NF-KB通过以前未知的机制介导炎症和抗细胞凋亡信号通路的激活。ZHX2与经典NF-KB亚基p65组成复合体,在多个DNA位点(以组蛋白H3 Lys4三甲基化(H3K4me3)和组蛋白H3 Lys27乙酰化(H3K27ac)为标志)与NF-KB共同基序结合,调控NF-KB的转录活力。Zhang等人进一步证实,NF-KB信号传导的抑制减弱了ccRCC细胞的生长。值得注意的是,转录分析显示,NF-KB靶基因的表达增加与ccRCC中较差的患者存活相关。这些发现可以解释为什么ZHX2在ccRCC中过表达。
在Zhang等人之前,有团队使用VHL靶标筛选方法,发现NDRG3(NDRG家族成员3)是VHL的潜在靶标。NDRG3是一种氧调节蛋白,可以激活Raf-ERK(细胞外信号调节激酶)信号传导,从而促进肿瘤生长。缺氧肿瘤微环境中积累的乳酸直接与NDRG3结合,抑制脯氨酰羟化酶-VHL机制,并防止NDRG3被降解。Zhang等人进行的体外筛选旨在寻找在疾病发展早期稳定存在的蛋白质,因为VHL的双等位基因失活是最早的致瘤事件之一,仅发生在染色体3p丢失之后。然而,缺氧ccRCC肿瘤中的乳酸积累可能有助于稳定一些体外筛选未检测到的其它因子,毕竟体外筛选无法准确地模拟肿瘤微环境。值得注意的是,Zhang等人并未报道NDRG3是VHL底物。将来我们可以在缺氧细胞开展这种筛选操作,寻找乳酸积累下游的蛋白质修饰。这将更密切地反映晚期疾病,包括肿瘤缺氧。
目前的一大难题在于将患者分层,使其更能从靶向治疗中受益。最近人们在对ccRCC患者分型上取得了重要进步:polybromo 1(PBRM1)基因丢失的患者更可能对免疫检查点阻断方法产生响应。然而,个性化地为患者选择小分子抑制剂仍然并非易事。基因组和临床前数据表明,抑制HIF2α在治疗大多数ccRCC患者中是有效的。然而,在实践中,HIF2α抑制对一些肿瘤不起作用,即使这些肿瘤表达HIF2α,而且最初对治疗敏感的肿瘤也会产生抗性。新兴策略的重点是确定ccRCC中可靶向的代谢适应,这可能有益于更大的、具有不同遗传背景的患者群体。这涉及多种代谢酶,尽管这些酶在ccRCC中普遍缺失,但我们可以使用表观遗传药物重新表达这些酶,从而改变ccRCC细胞的代谢,并杀伤肿瘤。生物标志物(例如ZHX2)的鉴定是一种新的患者分层方法——根据患者对肿瘤组合疗法的敏感度分层,并靶向新的临床可操作途径,例如NF-KB信号传导。然而,与大多数转录因子一样,目前要从药理学上抑制NF-KB还是有一定难度的。
Zhang等人的工作也提出了其它问题,包括:其它因素如何调节ZHX2蛋白的稳定性?可能存在其它非VHL依赖性机制调节ZHX2的稳定性,因为ZHX2蛋白的量并不总是与HIFα丰度相关,且恢复VHL表达后,ZHX2也未被完全降解。此外,由于ZHX2在某种程度上表达在VHL突变患者的肾上皮中,这种转录因子在ccRCC发展之前是否在健康肾组织中发挥作用?
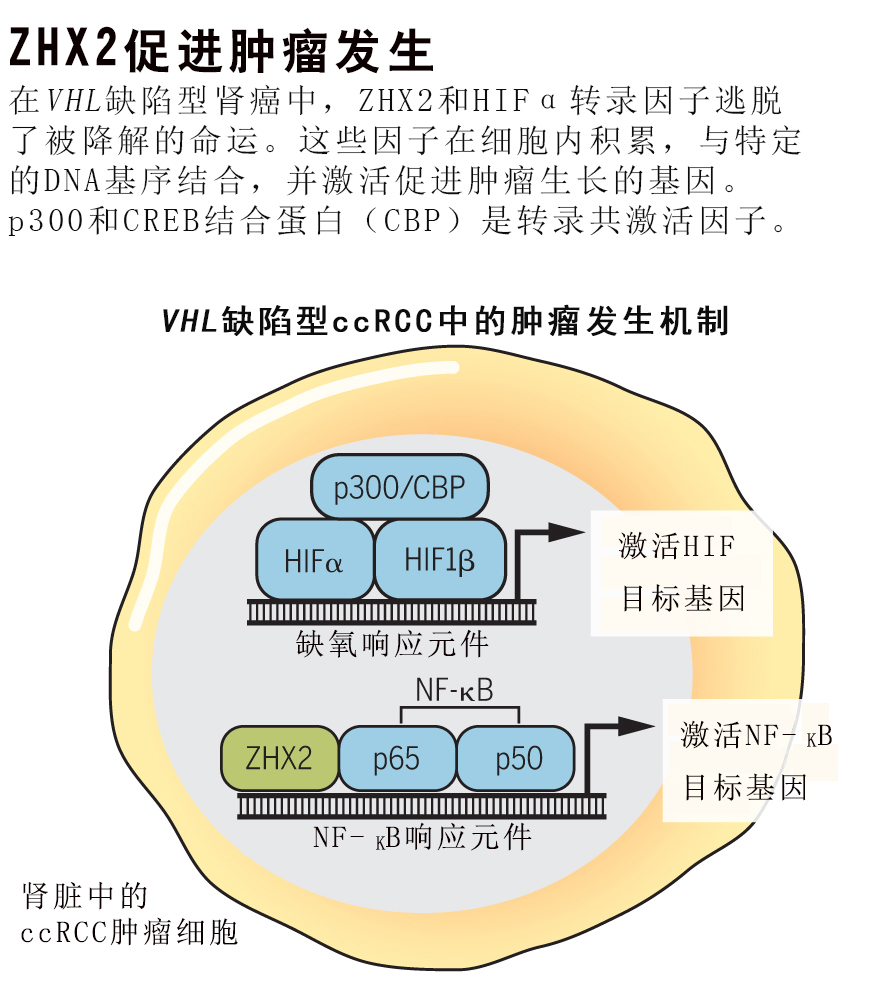
由于ZHX2和HIF2α分别调节ccRCC的不同的靶基因,所以它们很可能在肿瘤发生中具有互补作用(图“ZHX2促进肿瘤发生”)。此外,NF-KB下游的、负责促进ccRCC生长的关键途径和机制还未确定。鉴于敲除ZHX2仍然无法完全改善肿瘤生长,未来需要研究ZHX2敲除下游的细胞生长表型。此外,在较大患者群体中评估ZHX2的过表达及其后果也具有重要意义。
在肝细胞癌和霍奇金淋巴瘤中,ZHX2是一种肿瘤抑制因子,机制是转录抑制细胞周期蛋白A和E的表达。这与其在ccRCC中的作用形成对比,在ccRCC中ZHX2通过其在NF-KB靶基因表达中的积极作用来促进肿瘤发生。未来一个有趣的研究方向将是研究ZHX2在各种肿瘤中的表达和功能。这些研究强调了在确定给定分子是否具有致癌或肿瘤抑制作用时谱系特异性的重要性。
原文检索:
Danielle J. Sanchez. (2018) Transcriptional control of kidney cancer. Science, 6399:226-227.
张洁/编译