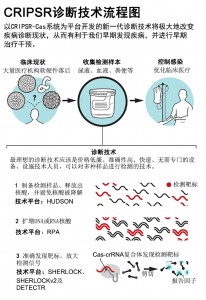
以CRISPR技术为平台打造的新一代诊断技术
CRISPR-Cas技术的出现,使得我们有望开发出一种新型的、快速而且准确的便携式诊断设备。
快速且准确的诊断感染性疾病是提升临床诊疗水平,以及指导感染性疾病防控和公共卫生工作,避免疫情大范围传播的关键,这一点无论对于现代化的大型医疗中心,还是在缺医少药的偏僻乡镇医院,都是非常重要的。最理想的诊断方式应该是价格低廉、准确性高,并且是快速的,而且还应该操作简便(无需专业人士操作即可使用),以及无需专业设备和基础设施要求(比如电力等条件)。对于埃博拉病毒(Ebola virus)和中东呼吸综合症病毒(Middle East respiratory syndrome coronavirus)这类出现在偏僻地点,但会导致全球大范围传播的致病性病毒而言,如果有了这种理想中的检测技术,就能够帮助医务人员在早期发现患者,将其隔离,避免疫情扩散,同时也可以给患者争取到更多及时治疗的机会。
研究发现,细菌和古生菌(archaea)等原核生物(prokaryotes)都具有先天的适应性免疫机制(heritable adaptive immunity),而这套免疫系统都是以最近非常热门的基因编辑技术CRISPR-Cas系统为基础的。近期《科学》(Science)杂志已经介绍了Chen科研团队、 Myhrvold科研团队和Gootenberg科研团队的工作。他们分别利用CRISPR-Cas技术开发了革命性的分子诊断新技术,以用于发现人体标本里的寨卡病毒(Zika virus, ZIKV)、登革病毒(Dengue virus, DENV)和人乳头瘤病毒(human papillomavirus, HPV)。同时他们也以肺癌患者的循环DNA(circulating cell-free DNA)为标本,对基因突变这类非传染性致病因素进行了诊断。
原核生物在它们基因组的CRISPR位点里储存了大量的感染性病原体(比如噬菌体、质粒和转座子等)的遗传信息,这些遗传信息就是原核生物自身的“抗体(适应性免疫记忆)”。Cas蛋白通过适应(adaptation)、转录出crRNA和干扰(interference)等步骤,完成原核生物的适应性免疫反应。在适应阶段,外源性遗传物质被原核生物加工处理及挑选,最后整合进CRISPR位点,打下深刻的免疫记忆烙印,为今后再次遭遇该感染源做好准备。前体crRNA是一种长链RNA前体分子,它成熟成为crRNA之后,可以指引Cas蛋白剪切外源遗传物质的互补链,这就是干扰步骤,最终使外源遗传物质降解,消灭外来感染源。科研人员彻底弄清楚这一套原核生物免疫机制之后,就开发出了新的分子诊断技术。
Chen的课题组发现,当CRISPR-Cas12a蛋白以序列特异性方式切割dsDNA时,还会诱导出很强的非特异性ssDNA反式切割效应(trans-cleavage)。根据这种特点,他们开发出了一种以临床常规采样标本为检测对象,快速鉴定HPV16、18型致癌病毒的新技术。通过肛门拭子(anal swabs)标本提取出HPV病毒的dsDNA,经过等温预扩增(isothermal preamplification),然后利用重组多聚酶扩增法(recombinase polymerase amplification, RPA)进行扩增。这种DNA扩增技术是一种快速,而且不需要专门仪器的DNA扩增技术。接着,他们通过Cas12a-crRNA复合体与扩增的HPV dsDNA结合,将其降解,同时诱发dsDNA反式降解反应,以激活结合在dsDNA分子上的荧光报告因子(fluorescent reporter),发出荧光,完成整个检测。这种新型诊断技术名为DNA内切酶靶向的CRISPR反式报告检测系统(DNA endonuclease-targeted CRISPR trans reporter, DETECTR)。该技术可以用来快速、且准确地检测各种亚型的HPV病毒。而且由于其快速、准确、便捷的特点,尤其适合世界卫生组织推荐的大规模普查工作。
Myhrvold等人开发的检测方法则是将采自患者的临床检测样品里的病毒核酸直接释放出来进行检测,略过了常规检测工作中的核酸提取这个步骤。这种方法被称作不经核酸提取热处理样品灭活核酸酶技术(heating unextracted diagnostic samples to obliterate nucleases, HUDSON)。这种技术能够大量灭活人体体液里的核糖核酸酶(ribonucleases),同时也可以使病毒的衣壳破裂,释放出病毒的核酸分子。Myhrvold等人还使用了以Cas13蛋白为基础的核酸检测技术平台——特异性高灵敏度酶报告系统(specific high-sensitivity enzymatic reporter unlocking, SHERLOCK)。与DETECTR系统类似,SHERLOCK系统也利用了RPA和Cas13蛋白,诱导出(非CRISPR)核酸切割反应。
在SHERLOCK系统里,结合了荧光报告因子的RNA被切割之后会释放出荧光信号,该荧光信号再经酶的放大,从而极大地提高了这种检测方法的灵敏性。Myhrvold等人将HUDSON技术和SHERLOCK系统结合起来,开发出了一种高灵敏同时高特异性的检测方法,可用于直接对体液(包括尿液、血液、唾液、血清和血浆等)中的登革病毒和寨卡病毒进行检测,在1至2个小时内给出检测结果。而且样品的制备过程也很简单,同时也不需要很复杂的设备。在中南美洲的很多地区,登革病毒和寨卡病毒都非常常见,而且临床表现也都差不多。如果孕妇感染了寨卡病毒,那么将极容易产下先天畸形的孩子,而且这种病毒可性传播,因此对孕妇和她们的丈夫进行检测就显得尤为重要。这套HUDSON——SHERLOCK检测技术可以很好地区分登革病毒、寨卡病毒、黄热病毒(yellow fever virus, YFV)这些在巴西多地流行,并导致严重疫情的病原体。该技术还可以很好地区分四种不同亚型的登革病毒,还能够对不同的寨卡病毒进行单核苷酸多态性(single-nucleotide polymorphisms, SNP)分析。这种功能可被用于多种SNP分析,比如耐药相关SNP、毒力相关SNP、传染性相关SNP等,从而帮助我们发现,并跟踪新出现的病原体。Myhrvold等人还将SHERLOCK报告系统的荧光信号改造成了类似于早孕试纸条式的报告系统,这非常适合在检测现场(point-of care)使用。
Gootenberg团队使用的也是SHERLOCK技术,不过他们对其进行了改进,开发出了SHERLOCKv2检测系统。这种系统只需通过一次反应便可同时检测三种ssRNA靶标和一种dsDNA靶标。他们对17种CRISPR-Cas13a酶和CRISPR-Cas13b酶进行了生化检测,然后从中挑选出3种有特殊切割活性的酶,再辅以Cas12a酶及RPA系统,最终开发出了这种能够在90分钟内同时检测寨卡病毒ssRNA、人工合成ssRNA(synthetic ssRNA)、登革病毒ssRNA,以及人工合成dsDNA的检测系统,而且检测结果还是容易判读的可视化结果。这种能够同时检测RNA和DNA的SHERLOCKv2技术非常适合用于肺炎致病病原体的鉴定。我们知道肺炎是全世界幼儿死亡的首要病因。不论是DNA病毒或者RNA病毒感染,还是同时合并了细菌感染导致的肺炎,都可以通过这种方法进行检测。这种便捷、廉价、方便的就地肺炎诊断技术一定可以帮助偏远地区的肺炎患者及早获得相应的(抗菌或抗病毒)医疗救助。
另外一种SHERLOCKv2技术可以对靶标进行高灵敏度的定量检测。这种简便而又准确的检测技术可以对医疗资源相对落后的地区的艾滋病患者进行HIV病毒滴度监测,以判断抗病毒疗法的疗效,从而改善艾滋病患者的诊疗状况。这种SHERLOCKv2技术还可以用来检测非小细胞肺癌患者血液中的DNA分子的突变情况,检测结果可以是荧光读数,也可以是侧向流免疫层析(lateral flow assays)方式,因此也可以用于液体活检(liquid biopsy)。Gootenberg团队在体外概念验证试验中,还成功应用SHERLOCKv2技术开展了基因编辑治疗,纠正了结肠癌突变基因,同时也利用SHERLOCKv2技术确定了被成功修复的突变基因的数目。
这些新开发的诊断技术还需要与传统检测技术进行对比,以确保它们的灵敏性和特异性,同时还需要进行现场测试,看看是否满足临床检测需要,因为不同检测环境,以及不同操作者都有可能影响检测结果。一旦通过了这些测试,这些新型的检测技术就可以投入实际应用,提高偏远地区的诊疗水平。在那些医疗条件落后的地区,不明原因发热的诊治是最常见,又是最难诊治的,这些疾病也是死亡率很高,传播范围很广的疾病。比如,每年全世界因为结核杆菌感染会使130万人死亡,因此结核病也是死亡率最高的疾病,而早期发现、早期处置其实是可以避免这些患者死亡的。
这些检测技术既可以用来研究致病病原体的耐药问题,指导临床用药;也可以分析致病病原体的活力(viability),以指导感染疾病的防控工作;还可以扩展检测范围,让粪便、呼吸道分泌物、脑脊液等标本都成为检测样品,以用于明确肠炎(enteritis)、肺炎(pneumonia)和脑膜炎(meningitis)等疾病的病因。随着技术的发展,根据准确性、可靠性、简便性、检测速度、灵活性、费用等方面的考虑,还可以将这些检测技术应用于传染性疾病和非传染性疾病的检测,也可以应用于临床、实验室,以及野外等多种场合。
原文检索:
Daniel S. Chertow. (2018) Next-generation diagnostics with CRISPR. Science, 360: 381-382.
Eason/编译